Anotace
Je podán výklad dopadu poruch funkce ledvin jako klíčového orgánu na udržování homeostázy vnitřního prostředí organismu a v orgánových soustavách s ledvinami regulačně spřažených (kardiovaskulární systém, kostní metabolismus, hemopoéza) nebo na funkci ledvin závislých (centrální nervový, gastrointestinální systém).
Definice
Selhání ledvin je porucha klíčového orgánu pro udržování vodní, elektrolytové a acidobázické homeostázy s bezprostředním dopadem na bazální buněčný metabolismus, na krátkodobou i dlouhodobou regulaci krevního tlaku a na funkce orgánových systémů závislých na regulačních funkcích ledvin v oblasti kalcium fosfátového (kostního) metabolismu, hemopoézy a metabolismu proteinů. Ledviny jsou limitním orgánem pro eliminaci řady katabolitů a cizorodých látek (léků, toxinů).
Etiopatogeneze ledvinového selhání
Východiska
1. Klíčové postavení ledvin v regulaci homeostázy s bezprostředním dopadem při výpadku funkce na bazální buněčný metabolismus změnami
- vodní rovnováhy,
- elektrolytové (Na+, K+, Cl-, fosforečnany, Ca2+, Mg2+ aj.) rovnováhy,
- acidobazické rovnováhy.
2. Nenahraditelné postavení
- při eliminaci základních proteinových katabolitů (urea, kreatinin, cystatin,…), v bilanci minerálů (natrium, kalium, chloridy) a řady cizorodých látek (léků, toxinů)
- v neurohumorálních regulacích (endokrinní funkce)
- při krátkodobé a dlouhodobé regulaci objemu ECT a krevního tlaku (systém renin-angiotenzin-aldosteron, efektor pro antidiuretický hormon),
- při regulaci kalciumfosfátové homeostázy, účast na metabolismu vitaminu D s dopadem na kostní metabolismus,
- při krvetvorbě (produkce erytropoetinu),
- renální prostaglanginy významnou mírou ovlivňují nastavení intrarenální cirkulace (vazodilatační efekt v juxtamedulárních glomerulech při hypotenzi) a pravděpodobně zasahují v případě jejich dysbalance prostřednictvím tubulárních funkcí do celkové vodní a elektrolytové rovnováhy (např. retence vody jako nežádoucí efekt nesteroidních antiflogistik),
- při metabolismu aminokyselin (reabsorbce aminokyselin v proximálním tubulu); v ledvinách se syntetizují aminokyseliny histidin a tyrosin, které jsou tímto fakultativně esenciální.
- ledviny rovněž hrají významnou roli
- při metabolismu glycidů – ledviny významnou mírou podílí na glukoneogenezi (z 1/3 veškerého objemu glukoneogeneze), významně utilizují glukózu (glykolýzou), mají minimální zásobu glykogenu;
- při metabolismu lipidů – v ledvinách se masivně oxidují mastné kyseliny (energetický zdroj pro ledviny, stimulují transport – eliminaci organických aniontů) a vychytávají ketokyseliny (acetoacetát).
3. Porucha funkce ledvin má vždy komplexní charakter, zasahuje vždy více jejich fyziologických funkcí a má dopad na více orgánových systémů.
- Ledviny mohou být primárním (prvotním) zdrojem poruchy.
- Častější je druhotná (sekundární) porucha funkce ledvin při onemocněních jiné orgánové soustavy – porucha funkce ledvin ji pak eskaluje – prohlubuje. Příkladem je kardiorenální syndrom, resp. renokardiální podle prvotní poruchy.
Při nevratném selhání funkce ledvin se stírá důležitost mezi přimární a sekundární příčinou, která vyvolala ledvinnou poruchu, klinický obraz se řídí jen stupněm ledvinného selhávání.
4. Rozhodující na tíži projevů renální poruchy je
- úroveň (prerenální, renální, subrenální)
- kvantita postižení (počet postižených nefronů)
- typ postižení nefronu (glomerulární, tubulární, histologický typ postižení)
- časový faktor vývoje poruchy
- je důležitý pro uplatnění jak kompenzační hyperfunkce nepostižených reziduálních nefronů, tak pro reparativní změny poškozených nefronů s částečným obnovením funkce anebo jizvením – fibrotizací se zánikem funkce
- je rozhodující pro dynamiku klinických symptomů a laboratorních markerů funkce ledvin vyplývající z pozvolného nástupu adaptačních procesů, zejména neurohumorálních maladaptací s dopadem v ostatních orgánových soustavách.
Etiopatogenetické mechanismy renálně podmíněných poruch vnitřního prostředí a orgánových soustav
Podle úrovně působení vyvolávající příčiny a z hlediska funkce ledvin před vznikem onemocnění je účelné rozeznávat poruchy funkce ledvin:
- prerenální(tabulka 1);
- (intra)renální (tabulka 2);
- postrenální (tabulka 3).
Prerenální příčiny poruch funkce ledvin
Jsou shrnuty v tabulce 1.
| Tabulka 1. Prerenální (extrarenální) příčiny poruch funkce ledvin (akutní i chronické) |
| Hemodynamické příčiny |
| Absolutní hypovolémie (dehydratace, krvácení, popáleniny, průjmy; hypovolemický cirkulační šok) |
| Ascites (onemocnění jater, malignity) |
| Relativní hypovolémie se snížením efektivního objemu cirkulující krve (redistribuce krve), např. anafylaktický šok, endotoxinový šok, septický šok, SIRS, MOF |
| Hepatorenálnísyndrom |
| Pokročilé srdeční selhání – kariogenní šok, kardiorenální syndrom |
| Postižení renálních cév |
| Uzávěr /stenóza a.renalis – trombóza/embolie |
| Poléková porucha intrarenální cirkulace – ACEi, AT1 |
| Uzávěr /stenóza v. renalis – trombóza v. renalis |
Rozhodující je dostatečný průtok krve ledvinami. Je zajišťován a. renalis a jejími větvemi, přívodní cévou (vas afferens) před každým glomerulem. Krev opouští glomerulus cestou vas efferens a větvemi ledvinných žil vtéká do dolní duté žíly. Kolísání průtoku přívodní a. renalis (resp. vas afferens) ovlivňuje filtraci přes glomerulus, a tím objem vylučované moče a funkci celého nefronu. Stejně tak je tvorba moče ovlivněna aktuálním průsvitem vas efferens – konstrikce vede ke zvýšení, vazodilatace ke snížení filtrace.
Ke snížení průtoku a. renalis dochází velmi často. Nejčastější příčinou je redistribuce krve při tzv. „centralizaci oběhu“ při pokročilém srdečním selhávání (kardiorenální syndrom), šokových a dalších stavech (dehydratace u starších lidí), kdy působením vyplavujících se katecholaminů a angiotenzinu dojde ke spasmu drobných intrarenálních vas afferens i efferens a ledvina (zejména její korová část) je ischemizována. Navíc se velmi často lokálně uplatňují progredující aterosklerotické (a následně trombotické) uzávěry. Akutním stavem je např. embolie přívodných renálních tepen (ateromové pláty z aorty anebo srdeční tromby).
Obdobný mechanismus je třeba zmínit při akutním renálním selhání při nevhodné léčbě ACE inhibitory na terénu snížené vaskulární rezervy ledvin (stenózy a. renalis, pokročilá nefroskleróza, či diabetické postižení). Zde při léčbě ACE inhibitory vede vazodilatace vas efferens ke snížení glomerulárního filtračního tlaku, a tím i glomerulární filtrace, funkce celého nefronu. Dochází k ochuzení prokrvení kůry ledvin ve prospěch prokrvení ledvinné dřeně.
U všech výše zmíněných stavů pak dochází ke globální (neselektivní) poruše ledvin vlivem poklesu glomerální filtrace. Ischémie dosti často vede k ischemické nekróze tubulů. Projevem je oligurie a s tím spojený nárůst kreatinémie a dalších N-katabolitů, metabolická acidóza, riziko hyperkalémie.
Renální příčiny poruch funkce ledvin
Jsou shrnuty v tabulce 2.
| Tabulka 2. Renální příčiny poruch funkce ledvin (akutní i chronické) |
Glomerulární příčiny (glomerulopatie)
|
| Primární |
| Glomerulonefritidy |
| IGA nefropatie |
| Sekundární – při systémových nemocech |
| Hypertenze |
| Henoch-Schonleinova purpura |
| Vaskulitidy |
| SLE, SCLE, Goodpastureův syndrom, Sjögrenův syndrom, kryoglobulinemie, sarkoidóza |
| Infekce (streptokokové) |
| Trombotická mikroangiopatie (HUS, HELLP) |
Tubulární příčiny (tubulopatie)
|
| Primární |
| Akutní a chronická infekce, tubulointersticiální infekce |
| Dědičné tubulopatie |
| Sekundární |
| Při poruchách prokrvení ledvin, |
| Infekce – sepse |
| V rámci systémových (multiorgánových) nemocí |
| Intratubulární depozice proteinů (rabdomyolýza, inkompatibilní krevní transfúze) |
| Iintratubulární deposice krystalů (např. kyselin močové – po rozpadu nádorů) |
| Aseptické tubulointersticiální nefritidy (léky, jedy) |
| Smíšené (glomerulární i tubulární) |
| Sekundární |
| Diabetes mellitus |
| Amyloidóza |
| Paraproteinemie při monoklonálních gamapatiích |
| Rejekce po transplantátu |
| Dědičná postižení ledvin (hlavní zástupci) |
| Polycystóza ledvin (ledvin a jater) |
| Wilmsův tumor |
| Fanconiho sy (dědičné formy) |
| Fabryho choroba |
| Alportův syndrom |
| Dědičné poruchy transportu iontů a vody |
| Hypertenze – dědičné formy (např.Liddleův syndrom) |
| Renální tubulární acidóza (RTA I, II) |
| Bartterův syndrom |
| Gitelmannův syndrom |
| Pseudohypoaldosteronismus |
| Nefrogenní diabetes insipidus |
Ledvina může být zčásti anebo zcela destruována nádorem. Nefrolitiáza se uplatňuje prostřednictvím blokády odtoku moče, přidruženými záněty ledvinného intersticia s prvotním narušením tubulární funkce ledvin; v terminální fázi se vyvíjí svraštělá ledvina s obrazem globálního selhání její funkce.
Poškozením funkčního parenchymu (masy nefronů) se snížením až zánikem funkce některých částí nefronu může dojít buď k výpadku funkce celého nefronu, nebo jeho části. Podle převažující lokalizace postižení v rámci nefronu lze pak patologické procesy rozdělovat na poruchy glomerulární a tubulární.
1. Glomerulopatie
Nejčastějšími glomerulopatiemi stavy jsou metabolicky podmíněná postižení při diabetu mellitu, ateroskleróze a záněty glomerulů – glomerulonefritidy. Podrobná laboratorní a histologická diagnostika má zásadní význam pro léčbu. Manifestace ve vnitřním prostředí a orgánových soustavách je víceméně jednotná. Ovládá ji masa a rychlost vzniku glomerulárního postižení a stupeň poruchy základní glomerulární filtrační funkce.
Dominantním projevem glomerulopatie je ztráta semipermeability glomerulární membrány. Projevuje se masivní proteinurií a následnými hypoproteinemickými otoky, neurohumorální aktivací RAAS s hypertenzí, možností ischemizace ledvin vlivem redistribuce krevního průtoku, s retencí vody a s metabolickým dopadem (hyperlipoproteinémie). K plnému rozvinutí stavu do obrazu nefrotického syndromu dochází zejména u chronických proteinurií. Hypoproteinémie není jedinou příčinou stavu, ale spolupodílí se na ní retence iontů sodíku a vody a snížená odpověď na atrální natriuretický faktor.
U akutních glomerulonefritid současně bývá vedle mírné proteinurie přítomen různý stupeň hematurie s anemizací (nefritický syndrom).
Poškozené glomeruly se hojí jizvením, tubuly jsou tímto afunkční, nefron zaniká. Terminálním obrazem chronické glomerulonefritidy je malá svrašťující se afunkční ledvina s reziduálním poškozeným prokrvením, podílející se tímto na udržování a další akceleraci sekundární renoparenchymální hypertenze.
2. Tubulopatie
Hlavními tubulárními onemocněními jsou bakteriální záněty a aseptické (sterilní) záněty ledvinného intersticia (tzv. tubulointersticiální nefritidy, nejčastěji při abúzu analgetik) a akutní tubulární nekróza. Nemalá část tubulárních poruch má genetický podklad. Selektivitu postižení tubulární funkce určuje typ defektu.
Zdrojem tubulární poruchy je pravidelně ischémie ledviny. Příčinou může být akutní uzávěr ledvinných cév, nejčastějším mechanismem je však redistribuce cirkulace při hypotenzívních a hypovolemických stavech (klasicky dehydratace, šok jakéhokoli původu), či jako nežádoucí účinek léků (ACE inhibitory) v těsné vazbě na výchozí stav ledvinných funkcí následkem chronických komorbidit.
Akutní tubulární nekróza vzniká také přímým toxickým účinkem cizorodých látek (etylenglykol – Fridex, houby – pavučinec plyšový, závojenka olovová), a pokud vůbec dojde k reparativní fázi, pak vždy poškození pokračuje intersticiální fibrózou s postupným selhá(vá)ním funkce ledvin.
Akutní tubulární nekróza se může vyvinout po podání kontrastních látek při rentgenovém a NMR vyšetření (kombinovaný efekt toxický a osmotický) u stavů s poruchou prokrvení nebo funkce ledvin (nefroskleróza, dehydratace, hypotenze, koindicence s léčbou metforminem či ACE inhibitory, diabetická nefropatie s renální insuficiencí).
Příčinou tubulární poruchy či nekrózy může být i intratubulární proces při nadměrném vylučování některých látek s jejich intratubulární precipitací ve formě válců. Precipitace může probíhat i intracelulárně při buněčném transportu v tubulárních buňkách. Tímto mechanismem se vyvíjí tubulární nekróza a intratubulární válce myoglobinu při rabdomyolýze. Jde o stav vyvolaný rozpadem svalů (rhabdomyolýza) po zhmoždění (crush syndrom) nebo jako poziční trauma u osob starých, v bezvědomí s prochladnutím, obecně častěji u alkoholiků, nebo při myositidě u systémových nemocí pojiva. Obdobný stav nastává při sekundární těžké hyperurikémii po rozpadu nádorových buněk při chemoterapii.
Zánětlivý proces či nekróza tubulárních buněk ve fázi reparace může vedle obnovení plné tubulární funkce pokračovat do intesticiální fibrózy se zánikem tubulární funkce, a tím i nefronu. Stejně jako u glomerulopatií je při nevratném tubulárním postižení velkého rozsahu klinická symtomatologie jednotná a řídí se stupněm globálního ledvinného selhání se všemi jeho atributy (viz níže o globálním výpadku ledvinné funkce).
Podle lokalizace funkční tubulární poruchy rozeznáváme typ proximální a distální. Hlavním představitelem proximálního typu je Fanconiho syndrom. Poruchy na úrovni distálních tubulů mohou mít povahu selektivního deficitu (např. distální renální tubulární acidóza, nefrogenní diabetes insipidus), častěji však jsou součástí globálního výpadku tubulární funkce po proběhlé ischémii anebo destrukci zánětem s intersticiální fibrózou. Jednotlivé tubulární funkce a jejich poruchy jsou probrány níže (odstavec Adaptační procesy při dlouhotrvající a progredující poruše renálních funkcí.)
3. Smíšené poruchy glomerulů a tubulů
K současnému glomerulárnímu i tubulárnímu poškození dochází při infiltrací patologickými látkami nebo metabolity. Dochází k nim zejména při monoklonálních gamapatiích (nejčastěji mnohotný myelom, B-lymfomy a leukémie). Lehké řetězce imunoglobulinů anebo jejich fragmenty tvoří intratubulární depozita ve formě válců (myelomová ledvina) nebo precipitují jako krystaly v tubulárních buňkách (při Fanconiho syndromu, cystinurii apod.), mohou být přítomna patologická depozita látek v bazální membráně glomerulů i tubulů, v mesangiu (nemoc lehkých řetězců). Stejně tak při sekundární amyloidóze jsou v glomerulu depozita amyloidu lokalizována v mesangiu, v oblasti bazální membrány, posléze infiltrují peritubulární struktury a vedou k vývoji intersticiální fibrózy. AA amyloid se v dnešní době antibiotik a minoritně objevujících se specifických zánětech tvoří při chronických procesech v rámci revmatoidní artritidy, při chronických střevních zánětech onemocnění, tuberkulóze. Při primární amyloidóze dochází vedle infiltrace funkčních struktur nefronu ke kondenzaci amyloidových fibril i ve stěně velkých i malých intrarenálních cév s jejich uzávěrem.
Subrenální příčiny poruch funkce ledvin
Jsou shrnuty v tabulce 3.
| Postrenální příčiny poruch funkce ledvin (akutní i chronické) |
| Blokovaná ledvina (obstrukční uropatie) |
| Urolitiáza |
| Nefrolitiáza |
| Ureterolitiáza |
| Cystolitiáza |
| Útlak ureteru |
| Tumory gynekologické, colon |
| Hypertrofie prostaty |
| Vezikoureterální reflux |
| Vezikoureterální reflux |
Blokádou odtoku moče močovodem – tzv. obstrukční uropatií – je zastaven odtok moče z ledviny, která secernuje moč do pánvičky. Vzniká její dilatace – tzv. hydronefróza, posléze se zastaví i funkce tubulární. Takto podmíněná anurie se vyskytuje nejčastěji při pokročilém zvětšení zvětšení prostaty nebo ucpání močovodu kamenem, či útlakem močovodu nádorem v okolí (tumory gynekologické a tlustého střeva).
Adaptační procesy při dlouhotrvající a progredující poruše renálních funkcí
Nedostatečná eliminace iontů sodíku, chlóru, draslíku a iontů H+ při nízké glomerulární filtraci, resp. diuréze, při chronickém selhání ledvin s podstatným snížením funkční masy nefronů podporuje výše uvedené stavy – retenci vody, oběhové přetížení až selhání srdce, acidózu. Hyperkalémie při chronickém i u akutním selhání ledvin vede k hyperpolarizaci membrán (neuromuskulární ploténky) se senzorimotorickými poruchami (třes, záškuby kosterních svalů, dysestésie končetin) a hlavně ohrožuje nemocné bradyarytmiemi, včetně zástavy srdeční. V pokročilých stadiích renálního selhávání, u akutních otrav podle vyvolávající noxy, se prohlubuje porucha acidifikace moče s retencí H+ a s metabolickou acidózu, se spotřebováváním bikarbonátové rezervy. Na acidóze se podílí i retence fosfátů a urátu zvyšujících schodek aniontů (anion gap). Klinickou manifestací stavu s významnou acidózou je kompenzační hyperventilace (acidotický foetor, Kussmaulův typ dýchání) při dráždění dýchacího centra H+ ionty, který částečně zmírňuje acidózu prostřednictvím vydýchávání CO2.
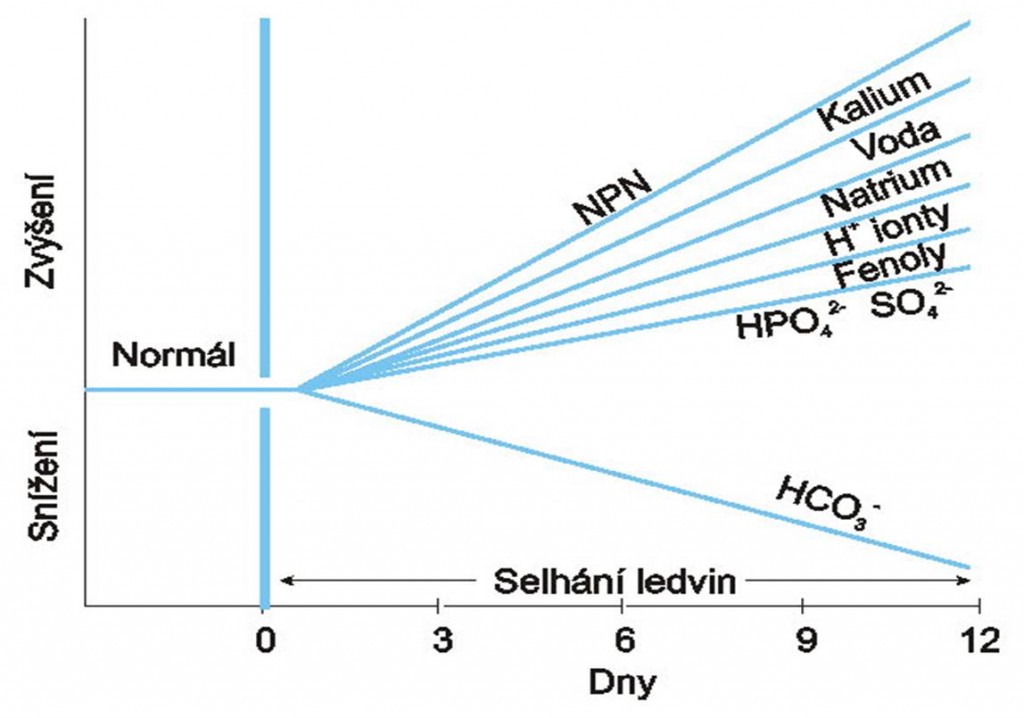 [1]
[1]Obr. 1. Kritické projevy akutního renálního poškození a renální insuficience ve vnitřním prostředí. NPN – neproteinový dusík (předeším kreatinin, urea a kyselina močová). (Podle AC Guyton a JE Hall: Textbook of Medical Physiology, 11th Ed. Elsevier/Saunders, Philadeplhia. 2006.)
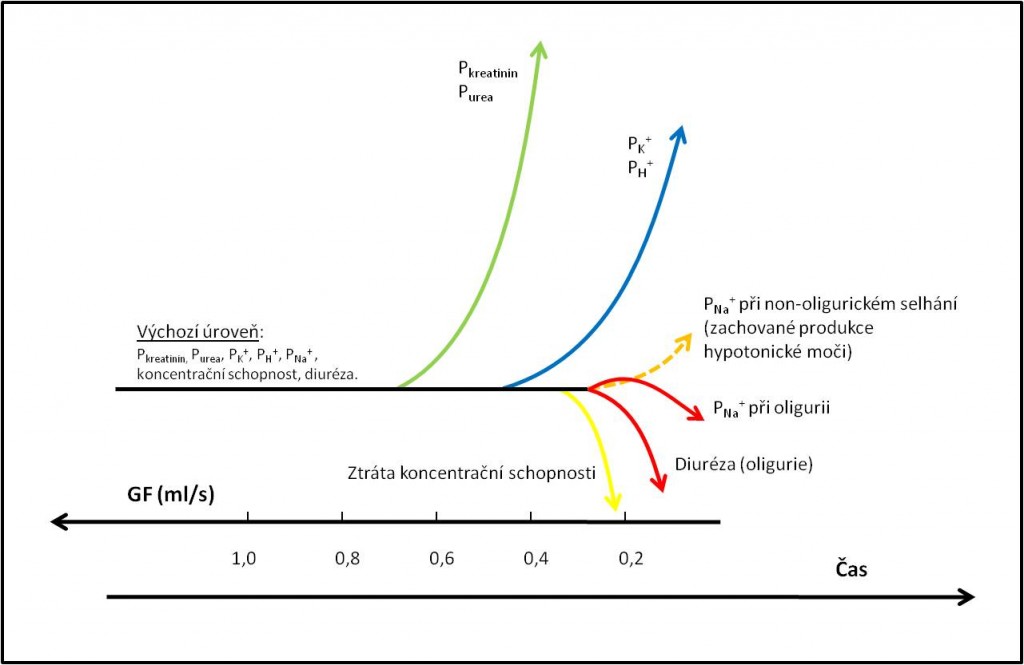 [2]
[2]Obr. 2. Postup změn při postupném zhoršování renálních funkcí. Změny biochemických ukazatelů v čase v závislosti na velikosti glomerulární filtrace. Pkreatinin, Purea, PK+, PH+ a PNa+ jsou plazmatické koncentrace uvedených solutů a iontů. Koncentrace kreatininu a urey v plazmě se začínají zvyšovat při poklesu GF pod asi 0,7 ml/s. Při poklesu GF pod asi 0,45 ml/s rostou koncentrace K+ a rozvíjí se metabolická acidóza. Při poklesu GF pod asi 0,3 ml/s ledviny ztrácejí koncentrační schopnost. Při oligurickém selhání zároveň ustává tvorba hypotonické moči, což je spojeno s přechodným zvýšením PNa+. Hodnota PNa+ se pak zpravidla s pozitivní bilancí tekutin snižuje, takže oligurické selhání bývá provázeno hyponatrémií. Při non-oligurickém selhání pokračuje tvorba hypoosmolální moči, takže non-oligurický stav může být provázen hypernatrémií. (Podle T. Zima a kol.: Laboratorní diagnostika, 2. vyd. Galén, Praha. 2007.)
.
Při akutních glomerulonefritidách se vyvíjí již výše zmíněný nefritický syndrom, při chronických glomerulopatiích s chronickými ztrátami bílkovin se vyvíjí již výše zmíněný nefrotický syndrom.
Při chronicky probíhajících glomerulopatiích a tubulopatiích ve fázi pokročilého selhání ledvin – na rozdíl od akutního selhání – je přítomen časový prostor pro uplatnění adaptačních procesů na vzniklou poruchu a dochází k rozvoji tzv. uremického syndromu a neurohumorálních maladaptací.
Uremický syndrom je komplex příznaků multiorgánového postižení při chronickém selhávání ledvin ve stádiu IV a V dle klasifikace K/DOQI (viz níže, tabulka 5). Dominantním patogenetickým mechanismem vývoje uremického syndromu je neschopnost ledvin vyloučit z organismu katabolity, minerální látky a tělu cizích látek, které jsou glomeruly filtrovány, dále zpracovávány za průchodu tubuly a odstraňovány močí. Tímto způsobem jsou eliminovány desítky nízko- a středněmolekulárních látek do velikossti Mr 58 000. Další, vysokomolekulární látky, jsou ledvinami metabolizovány. Při výpadku glomerulární či tubulární funkce se v organismu jinak běžně vylučované katabolity kumulují a buď samotné, nebo jejich další degradační produkty, působí toxicky na buněčný metabolismus. Působí také osmoticky (hyperhydratace tkání). V naprosté většině jde o katabolity obsahující dusík (tzv. N-katabolity). Hlavními sledovanými a odrážející globální funkci ledvin jsou urea, kreatinin a případně kyselina močová.
Kumulace iontů a katabolitů vede k metabolické acidóze, osmotické retenci vody v buňkách a v instersticiu. Vyjádřením tohoto působení na mozek jsou pak kvalitativně-kvantitativní poruchy vědomí, slabost, nauzea a zvracení. Může se objevit průjem. Dále plíživý nástup srdeční slabosti následkem objemového a tlakového přetížení. Hyperhydratace vede k hypertenzi. Ve vystupňovaném stavu se vyvíjí klasický obraz kardiálního astmatu, anasarka s pleurálními výpotky a s ascitem. Po stránce metabolické je terminálním stavem uremické koma s edémem mozku.
Mezi klasické projevy uremického syndromu patří perikarditida, suchá i exudativní, nejčastěji s hemoragickým výpotkem. Jeho hemodynamická významnost není vždy odrazem jeho množství, při plíživém průběhu nemocný toleruje i objemné výpotky.
Významnou poruchou při chronickém selhání ledvin při eliminaci minerálů je neschopnost ledvin v dostatečné míře eliminovat fosfáty se vznikem sekundárního hyperparathyroidismu. Retence fosfátů prohlubuje acidózu (zvyšuje se progresivně anion gap). Druhotně v rámci zachování Ca/P rovnováhy je v séru tendence k hypokalcémii, která provokuje zvýšenou sekreci parathormonu, v jehož důsledku je vyplavováno kalcium z kostí se vznikem výrazné osteoporózy, zvýšeně se ukládá v cévách (intima, média), subendokardu chlopní, měkkých tkáních, je akcelerována kloubní degenerace. Současně je hypokalcemizující proces podpořen absencí funkce ledvin provést hydroxylaci vitaminu D se vznikem aktivních metabolitů. Sekundární hyperparathyroidismus akceleruje difúzní aterosklerotický proces, kalcifikace v oblasti chlopní s časnějším vznikem degenerativních chlopenních vad (aortální, mitrální vady), svými cévními manifestacemi napomáhá k akceleraci paralelně se rozvíjející hypertenze (při aktivaci systému RAAS, volumdependentně při oligurii, atd.) s další eskalací účinků na cévní stěnu, myokard (uremická kardiomyopatie). Manifestací je více jak 10násobný nárůst CMP, koronárních příhod, náhlých úmrtí pacientů s chronickým selháním ledvin.
V této souvislosti lze zmínit, že primární hyperparatyreóza (primární adenom či karcinom příštítných tělísek) má projevy stejné jako právě popsaný sekundární proces, pouze s tím rozdílem, že extrarenální manifestace (z hyperkalcémie) předchází projevy renální. Typickým renálním následkem primárního hyperparatyreoidismu je nefrokalcinóza s tubulární poruchou, intersticiální fibrózou a druhotným selháním ledvin.
Kompenzací nedostatečné eliminace iontů je funkční přestavba reziduálních nefronů ve smyslu snížení tubulární resorbce sodíku, aktivní exkrece draslíku se vzestupem jejich frakční exkrece. Není-li narušena tato adaptační schopnost tubulů v reziduálních nefronech, může být vzestupem frakční exkrece sodíku a draslíku jejich vyrovnaná bilance zachována i při velmi nízkých hodnotách glomerulární filtrace. Maximální hodnoty frakční exkrece ukazuje tabulka.
Při tubulárních poruchách bývá pravidelně je porušena koncentrační schopnost ledviny – postupně se vyplavuje až mizí dřeňový koncentrační gradient, netvoří se hyperosmolární , ale izo- nebo hypoosmolární moč. Eliminace solutů (katabolitů, minerálů). Při poruše koncentrační schopnosti tubulů se zachovalou glomerulární funkcí se porucha manifestuje často jako polyurie a nemocný je ohrožen zejména dehydratací, hyponatremií a hypokalemií. U pacientů v polyurické fázi selhání ledvin (reparace akutního selhání ledvin, ztráta koncentrační schopnosti, přílišná diuretická léčba), je pacient ohrožen dehydratací s oběhovým zhroucením, hyponatrémií a hypokalémií.
Porucha tubulárního transportu aminokyselin (fyziologická je reabsorbce až 90 % aminokyselin v proximálním tubulu) vede k nežádoucí generalizované aminoacidurii, podílející se při chronickém průběhu na všeobecné proteinové malnutrici (viz též odstavec Fanconiho syndrom).
V rámci zániku funkcí nefronu dochází při chronické renální insuficienci k výpadku tvorby i účinnosti erytropoetinu, je zkráceno přežívání erytrocytů. Tímto dochází ke vzniku normocytární normochromní anémie. Současně je anémie podporována krevními ztrátami (opakované odběry, tendence ke krvácení do zažívacího traktu), nedostatkem železa (katabolická spotřeba, krevní ztráty), méně deficitem folátů a vitamínu B12 anebo komorbiditami – např. diabetem či hypotyreózou.
Po stránce koagulační je na podkladě změn v cévní stěně (akcelerace aterosklerózy) a při poruše destičkové funkce (vliv uremických toxinů) tendence k hemoragickým komplikacím – krvácení i po malém tramatu anebo spontánně do podkoží,do sliznic, subkonjunktiválně, serózní krvácení (hemoragizovaný perikardiální či pleurální výpotek, peritoneum), je zvýšená četnost krvácení z cévních malformací do CNS.
Na druhé straně je popsán vyšší výskyt trombotických příhod (např. embolie plicní, uzávěry žilních spojek pro dialýzu) se zvýšeným záchytem trombofilie pro funkční poruchu proteinu C, výskyt antifosfolipidových protilátek anebo hyperhomocysteinémii.
Po stránce endokrinní je při renálním selhání snížená degradace inzulínu (vedoucí u diabetiků léčených inzulinem ke snížení jeho spotřeby, hypoglykémiím). Je narušena přeměna tyroxinu v trijodtyronin, vzniká lehká hypotyreóza. Jsou známy poruchy růstu u dětí, způsobené porušenou tvorbou aktivního faktoru IGF-1. Dochází k poruchám pohlavních hormonů. Hyperprolaktinémie, nižší hladina testosteronu vede u mužů ke gynekomastii, sexuální dysfunkci, u žen s přispěním ztráty pulzatilní tvorby LH k dysmenoree a neplodnosti.
Je narušena imunitní odpověď na infekci na úrovni buněčné imunity s poruchou prezentace antigenů, což způsobuje vyšší tendenci k infektů, zejména jsou-li pacienti podrobováni častějším cévním punkcím (odběry) a kanylacím(hemodialýza). Z tohoto důvodu je i vyšší incidence malignit u dialyzovaných nemocných .
Malnutrice je dalším důsledkem uremického syndromu. Je uváděna hypotéza vlivu vysokomolekulárních látek: leptinu, ghrelinu, zánětlivých cytokinů. U leptinu je zdůrazňován vliv na pocit sytosti, aktivaci sympatiku a sekreci inzulínu. Ghrelin (tvorba žaludeční sliznicí) ovlivňuje chuť k jídlu. Spojitost malnutrice se zánětlivými cytokiny je dávána jako paralela s kachexií u jiných stavů, u nichž je výrazně zvýšena hodnota IL-6 a TNF, snižujících mimo jiné chuť k jídlu. Na malnutrici se podílí i nutné dietní omezení příjmu bílkovin u léčených pacientů a ztráty bílkovin proteinurií.
Klinický obraz
Klinický obraz při selhání ledvinných funkcí je pestrý a jeho projevy se řídí rozsahem a úplností postižení renálních funkcí a dobou, po kterou se porucha rozvíjí. Můžeme tak charakterizovat stavy s globálním (úplným) anebo parciálním (dílčím) výpadkem renální funkce, akutní a chronické renální selhání. Podle projevů lze rámcově rozlišit symptomy odpovídající vlastní renální poruše, kardiovaskulární projevy, projevy odpovídající již pokročilé metabolické poruše, přičemž není reálné jednotlivé symptomy od sebe oddělit, protože symptomy jsou často nespecifické a odpovídají komplexnosti poruchy.
1. Renální symptomy
Nejčastějším a dominantním příznakem renálního selhání je pokles diurézy, při poklesu pod 500 ml/den hovoříme o oligoanurickém selhání. Chronické stavy vyvíjející se plíživě mohou mít pokles diurézy jen pozvolný, nebo diurézu zachovanou a pak dochází hlavně k retenci dusíkatých katabolitů (neoligurické selhání), projevům acidózy, anémie, či sekundární hyperparathyreozy (kostní a kloubní projevy).
Lumbalgie jako další symptom je zejména u akutních stavů provokována otokem ledviny, městnáním moče v pánvičce při obstrukci močových cest, bolestivým spasmem ureteru při průchodu kamene. Cenným příznakem je současná hematurie, laboratorně s průkazem glomerulárního původu.
Dysurie (bolestivé močení) a polakisurie (časté močení) patří spíše k onemocněním dolních močových cest (cystitidy, prostatitidy, uretritidy), je cenným symptomem – upozorňuje na možnost sdruženého onemocnění ledvin s nutností ověření.
Vysoká horečka se zimnicí bývá přítomna u bakteriálních infekcí, nápadným rysem ukazujícím na možnost renálního zdroje je absence evidentního postižení jiných orgánů, často v konstrastu s těžkým celkovým stavem (např. u sepse). Hlavním markerem při klinickém vyšetření je podle typu prvotní příčiny např. neklid pacienta při renální kolice, bolestivé tapottement při akutní nefritidě (otok ledviny), hmatná elastická až tumorózní rezistence močového měchýře v podbřišku u retence močové, krvavý anebo hnisavý výtok z uretry apod.
2. Kardiovaskulární symptomy
Akutní i chronické selhání ledvin s poklesem diurézy vede k hyperhydrataci, anamnesticky se snažíme získat informaci o těchto projevech: nárůstu hmotnosti, délku trvání otoků, typu dušnosti.
Při klinickém vyšetření nacházíme zejména známky hyperhydratace s edémy, v případě nefrotického syndromu (hypalbuminémie) lokalizovanými často i v obličeji. Bývá patrná zvýšená náplň krčních žil, pravidelně je přítomna hypertenze.
Nejvýznamnějším projevem je kardiální manifestace formou levostranného či globálního srdečního selhávání. Je třeba si uvědomit, že pokud nejde o koincidenci se stavy po infarktu myokardu anebo při známé dilatační kardiomyopatii (DKMP), je srdeční insuficience podmíněna zejména diastolickou poruchou, po srdečním infarktu a při DKMP lze očekávat i systolickou poruchu (se sníženou kontraktilitou, resp. sníženou ejekční frakcí levé komory).
Při levokomorovém selhávání je klasicky manifestním příznakem námahová dušnost, ale nezřídka pacient přichází až s projevy plicního edému (ortopnoická dušnost, distanční difúzní vlhké plicní chropy, vykašlávání zpěněného sputa).
Globální srdeční selhávání se podle pokročilosti manifestuje dušností, otoky, anasarkou s pleurálními výpotky, ascitem.
V rámci kardiální manifestace bývají přítomny tachyarytmie (sinusová tachykardie, paroxysmální fibrilace síní), bradykardie může naznačovat přítomnou hyperkalémii s nebezpečím srdeční zástavy.
Při selhání ledvin se setkáváme s termínem kardiorenální syndrom, resp. renokardiální syndrom. Je to stav, kdy dysfunkce jednoho orgánu může vyvolat akutní nebo chronickou dysfunkci orgánu druhého. Symptomatologie se neliší od projevů každého jednotlivého orgánu, ale vždy je třeba při souhrnné diagnostice na tyto spojitosti myslet a podrobit tomu diagnostický a léčebný přístup.
Mezi kardiovaskulární projevy chronického selhání ledvin můžeme jednoznačně zařadit manifestní či nemanifestní projevy porušeného kalciofosfátového metabolismu se sekundární hyperparathyreoózou s kauzální vztahem k průkazným extraoseálním kalcifikacím v cévách, na chlopních, v měkkých tkáních. V tomto smyslu nejasné bolesti na hrudi, dušnost mohou být korelátem koronárního postižení, proto v anamnéze pečlivěji pátráme po souvislostech se zátěží, trvání, lokalizaci a iradiaci bolesti, spojení s dušností. Nezřídka jsme odkázáni při náhodném průkazu levostranné srdeční slabosti při fyzikálním nálezu na zobrazovací metody, neboť uremický pacient je často oligosymptomatický. Obdobně předvídavě přistupujeme ke klaudikačním symptomům dolních končetin: pátráme po poruše periferního prokrvení nohou (nehmatné pulzace na periferii a. tibialis posterior, a. dorsalis pedis, snížení indexu uzávěrových tlaků na dolních končetinách. Naopak známkou mediokalcinózy mohou být dobře hmatné periferní tepny, které jsou nekomprimovatelné manžetou tlakoměru při měření uzávěrových tlaků.
Obdobně u chronického selhání ledvin hodnotíme věku a anamnéze neodpovídající klasické projevy chlopenních vad, zejména aortální stenózy (námahová synkopa, stenokardie, dušnost), mitrální vady (převážně regurgitační vady – dušnost jako pozdní symptom) patří do obrazu sekundární hyperparathyreózy, stejně jako synkopy dané uzávěrovým postižením v oblasti karotického řečistě (ve fyzikálním nálezu s oslabením pulzací, popř. šelestem dostupné společné karotidy).
Závažným kardiovaskulárním syndromem chronického selhání ledvin je perikarditida, s možností manifestace retrosternální bolestí (třecí šelest), či jako dušnost anebo až pod obrazem srdeční tamponády (dušnost bez městnavých fenoménů na plicích, syndrom vtokové stázy s masivní náplní krčních žil, s tendencí ke kolapsovým stavům, je přítomen paradoxní pulz a tachykardie, hypotenze). Konstriktivní perikarditida s výraznou perikardiální fibrotizací a kalcifikacemi vede rovněž k obrazu syndromu vtokové stázy. Při hemodynamicky významné perikarditidě se lze setkat s městnavou hepatomegalií, otoky. Lze očekávat rovněž tromboembolické komplikace plicní.
Jindy může být jediným kardiovaskulárním projevem selhání ledvin anemický syndrom (únava, dušnost, stenokardie, posturální závrativost), uremický kolorit kůže (bledá, žlutozelená až slámová barva).
Při klinickém vyšetření potvrzujeme anamnestická data (pokud jsou dostupná) – poruchy chování a vědomí (únava, slabost, pocit dušnosti, bradypsychie, apatie, somnolence až koma). Při uremickém komatu je přítomno takřka vždy nápadné strojově pravidelné hluboké dýchání, uremický foetor a zápach potu. Gastrointestinálními projevy – nauzea a zvracení jsou časté, občasně je přítomen průjem. Hyperfosfatémie vyvolávající hyperparathyreózu způsobuje výrazný pruritus.
4. Ostatní symptomy
Renální osteopatie
Jde o zdánlivě nespecifické skeletální projevy, ale při povědomí léta probíhajícího ledvinného selhávání jde o základní symptomatický prvek zapadají do typického klinického obrazu sekundární hyperparathyreózy. Patří sem zejména projevy progredující artrózy nosných kloubů (bolesti kyčlí, kolen), osteoporotické bolesti a fraktury oblasti hrudní, bederní páteře a žeber, dlouhých kostí. Občasným nálezem je náhodný záchyt rtg měkkotkáňových kalcifikací. Kardiovaskulární projevy byly zmíněny výše.
Globální výpadek funkce ledvin
Akutní oligoanurické selhání funkce ledvin (diuréza do 150-500ml/den) – ve fázi počátečního poškození ovládají klinický obraz kardiovaskulární projevy z převodnění, závažnými jsou těžká metabolická acidóza, arytmie z hyperkalemie. Ve fázi tzv. časné diurézy s izostenurickou polyurií je nemocný naopak ohrožen zejména dehydratací s hypokalémií. Ve fázi pozdní diurézy a v reparativní fázi odpovídají jsou obtíže reziduální renální poruše.
Akutní neoligoanurické selhání ledvin – dominujícím příznakem jsou projevy metabolické a arytmie z hyperkalémie.
Závažným stavem jsou při akutním selhání ledvin centrální mozkové projevy z hyperosmolality při extrémní retenci osmoticky potentních a obecně pro buněčný metabolismus toxických dusíkatých katabolitů (urea) a vlivem metabolické acidózy. Vzniká edém mozku, zástava buněčného metabolismu s poruchami vědomí, oběhu a dechové aktivity. Typickým obrazem acidózy je strojově pravidelné hluboké dýchání (tzv. Kussmaulův typ), fungující jako kompenzační proces (výdej CO2). Při poškození vitálních center mezimozku v terminální fázi s útlumem dechového centra nastupuje periodický typ ventilace a dechová a oběhová zástava. V dechu je cítit uremický foetor.
Chronické selhání ledvin ovládá postupně se rozvíjející uremický syndrom: K plně rozvinutým metabolickým projevům (toxický vliv a hyperosmolalita při retenci dusíkatých katabolitů, acidóza) se přidávají projevy neurohumorální maladaptace (sekudární hyperparathyreóza, anémie, gastrointestinální projevy). Pro kardiovaskulární projevy (hypertenze, hypervolémie) je rozhodující stupeň hyperhydratace a zachovalost diurézy, tendence k hyperkalémii.
Parciální porucha funkce ledvin
Příznaky při stavech, které způsobují dílčí poruchu renálních funkcí, odpovídají etáži postižení (glomerulární, tubulární) a poškozené dílčí funkci. Časový faktor vývoje poruchy je určující stejně jako u globálního výpadku funkce pro rozvoj reparativních, resp. adaptačních (kompenzačních) změn ve funkci poškozených, resp. nepoškozených nefronů. Při progredujících anebo neléčených stavech s pozdní diagnostikou se rozvíjí klasický soubor příznaků ledvinného selhání (globální výpadek funkce), s manifestacemi již bez ohledu na prvotní příčinu poruchy (cévní, glomerulární, tubulární poškození) – stav končí obrazem afunkční malé svraštělé jizvící se ledviny.
Patří sem projevy glomerulárních onemocnění s proteinurií různého stupně, která při masivní či dlouhotrvající proteinurii vyvolává klasické projevy nefrotického syndromu (otoky, hypertenze, hyperlipidémie, snížení glomerulární filtrace), s hematurií (anemický syndrom). Glomerulární a tubulární poruchy s mírnými projevy bez vazby na jiné akutně celkový stav alterující onemocnění (infekce, otrava apod.) bývají asymptomatické a dlouho tolerovány, proto jsou často dominantním nálezem až projevy uremického syndromu s pokročilýmo hromaděním dusíkatých katabolitů (encefalopatie při hyperosmolarním stavu, toxické centrální vlivy) při jejich nedostatečné eliminaci do izostenurické moči při ztrátě koncentrační schopnosti ledvin. Jindy může být prvotní porucha eliminace kyselých katabolitů (genetické poruchy)s vystupňovanou acidózou (opět encefalopatie, poruchy dechového centra), poruchy minerálové dysbalance (hyperkalémie).
U všech chronicky probíhajících glomerulo- a hlavně tubulopatií se zřejmou poruchou jejich funkce se plíživě vyvíjí porucha kalciofosfátového metabolismu se sekundární hyperparathyreózou (klíčovým spouštěčem je porucha odstraňování fosfátů) s postupně plně vznikající uremickou kostní nemocí (renální osteopatií), kardiovaskulárními komplikacemi při extraoseálních kalcifikacích (cévní-masivní akcelerace aterosklerózy, chlopenní kalcifikace). Jeho mírné projevy pravidelně unikají pozornosti,významné manifestace pak napomáhají odkrytí celého spektra postižení – viz renální syndrom.
Celkové příznaky parciální poruchy funkce ledvin mohou často být jen velmi neurčité a jen hrubě odpovídat typu postižení (neupravující se únava, nevýkonnost, nastupující bradypsychie, poruchy diurézy, neurčité lumbalgie). Vodítkem pro provedení další diagnostiky může být potenciálně ledviny poškozující stav v anamnéze (např. horečnatý respirační infekt v odstupu s únavou, subfebriliemi, polyartralgiemi, otoky), příznakem může být nově zjištěná hypertenze) anebo je průběh němý až do fáze selhání renálních funkcí (abúzus analgetik). Jak již bylo zmíněno, některá onemocnění, zejména tubulární mají familiární výskyt se známým typem genetického postižení a rodinná anamnéza má zásadní význam (Alportův , Fanconiho syndrom, renální tubulární acidóza, Fabryho choroba, polycystóza a další).
Diagnostika poruch ledvin
Vyšetřovací diagnostické postupy se zásadním vztahem k ledvinám:
- Anamnestická data, klinické symptomy;
- Laboratorní vyšetřovací postupy;
- Zobrazovací a funkční přístrojové metody.
Anamnestická data, klinické symptomy
Zásadní anamnestickou informací je přítomnost diabetu a onemocnění s klíčovým vztahem k ledvinám: Urologická onemocnění, obecně onkologická onemocnění s intenzívní chemoterapií, riziková ATB léčba, podání rentgen-kontrastních látek, kontrastních látek při magnetické rezonanci, myelom, myositida, systémový lupus erytematodes, crush syndrom, předcházející hypotenze, hypovolémie anebo hyperosmolární stavy. V úvaze o intoxikaci má zásadní význam ne vzácná otrava etylenglykolem nebo houbami – pavunčincem plyšovým.
Klíčové symptomy ukazující na renální poruchu jsou:
- Změna vodní bilance (rychlé změny změny tělesné hmotnosti, diureza za posledních 24 hodin);
- Abnormální vzhled moče;
- Otoky a dušnost;
- Lumbalgie;
- Horečky, zimnice bez zřejmých orgánových symptomů;
- Zásadní změna chování.
Pátráme po specifických symptomech odpovídajících základnímu onemocnění (primárně postižené orgánové soustavě), které by renální poruchu mohlo druhotně způsobit.
Markery – vyšetřovací laboratorní postupy
Vzhledem k relativně chudé a nespecifické klinické symtpomatologii provázející ledvinné postižení je velký důraz ve screeningu kladen na laboratorní průkaz přítomnosti „nefropatie“. Při prvotním posouzení globální funkce ledvin má ve screeningu hlavní diagnostickou cenu průkaz oligoanurie a retence dusíkatých katabolitů, ostatní metody slouží k následné zpřesňující diagnostice.
Souhrn základních diagnostických funkčních laboratorní vyšetření ledvin:
- Globální funkce – diuréza, hladina dusíkatých katabolitů, mineralogram (Na, K, Cl, Ca, P), acidobázická rovnováha;
- Glomerulární funkce – glomerulární filtrace (MDRD, cystatinová nebo dnes nedoporučovaná kreatininová clearance), proteinurie, erytrocyty v zástinu při hematurii;
- Tubulární funkce – bilancovaná vyšetření močových odpadů vylučovaných minerálů (globální odpady/24 h, frakční exkrece), koncentrační schopnost, acidifikační funkce, odpady urey);
- Ostatní funkce – sekundární hyperparathyreoidismus (sérový parathormon), sérový erytropoetin, vitamin D.
Podrobný klinicko-laboratorní postup pro posouzení poruch ledvin
Jsou uvedeny obecné markery dopadu poruchy funkce ledvin ve vnitřním prostředí, současně pak speciální diagnostické testy, které směřují ke specifickým typům onemocnění a které nelze v rámci základní diagnostické baterie testů u poruch ledvin ignorovat.
Dpoporučuje se, aby základní laboratorní diagnostika byla vedena ve 2 krocích:
- Potvrzení, že jde o poruchu funkce ledvin;
- Co nejširší laboratorní záběr speciálních testů pro úspěšný záchyt specificky léčitelného základního onemocnění.
Ve specificky zaměřené následné diagnostice dopadu již zjištěných poruch renálních funkcí je klíčovým:
- Zjištění stavu a monitorace průběhu léčby abnormního kalcium-fosfátového metabolismu;
- Průběžné monitorování stavu minerálů natria, kalia a vodní diurézy, acidobazické rovnováhy a proteinurie;
- Určení stupně retence a monitorování obratu urey jako hlavního katabolitu závislého na funkci ledvin;
- Zjištění stavu a monitorace léčby směřované k normalizaci pochodů hematopoézy.
1. Je zavedeno monitorování bilance tekutin, minimálně diurézy, podle možnosti denní vážení – objektivizace oligoanurie (anurie – do 150ml, oligurie- pod 500ml)
2. Vyšetření moče
- Hustota (specifická hmotnost, sp. h.)
- Izostenurie – sp. h. kolem 1010 podporuje dg. parenchymového postižení ledvin, většinou velmi světlá moč;
- Hyperstenurie – sp. h. nad 1025, většinou tmavá moč, podporuje dg. extrarenální příčiny ledvinného selhání;
- Hypostenurie – sp. h. kolem 1002 – vyžaduje zahrnout do diagnostiky možnost deficitu ADH (diabetes. insipidus).
- Vyšetření hustoty moče lze nahradit vyšetřením osmolality.
- Index osmolalita moč/plasma:
- Pod 1,1 svědčí pro parenchymové onemocnění ledvin;
- Nad 1,5 svědčí pro extrarenální příčinu ledvinného selhání.
- Moč kvalitativně – Hematurie, bílkovina, Bence-Jonesova bílkovina, glykosurie, aceton, pH;
- Specifická – Porfyriny, oxaláty, myoglobin, toxikologická analýza;
- Moč kvantitativně – Proteinurie, odpady Na, K, Cl, poměr osmolality séra/moče, poměr sodíku moč/plazma;
- Specifická – Odpady Ca, P, kortizol, elfo bílkovin s imunofixací, odpad urey, exkreční frakce Na, K;
- Močový sediment bazální – počet erytrocyturie, leukocyturie, přítomnost krystalů a válců, bakteriurie;
- Močový sediment specificky – Vyšetření hematurie na průkaz glomerulárního původu, popis krystalů (uráty, oxaláty,..), válců, průkaz trichomonád;
- Vyšetření koncentrační schopnosti ledvin, popř. s podáním desmololu (syntetický ADH).
3. Krevní testy
- Základní:
- Urea, kreatinin, stanovení GF dle MDRD (obsolétní kreatininová clearance), fakultativně: cystatin (cystatinová clearance);
- Mineralogram (NA,K,CL,Ca,P,Mg), ABR, osmolalita séra;
- Markery zánětu – Krevní leukocyty, CRP, fakultativně: prokalcitonin.
- Obecné parametry krevního obrazu a koagulace (INR, PTT, kvantitativně D-dimery.
- Fakultativní testy podle uvažovaných orgánové souvislostí a speciální testy:
- Cystatin, cystatinová clearance, NGAL, IL-18, KIM-1 – citlivější markery renálního postižení předcházející elevaci kreatininu, nejdostupnější je cystatin C;
- Rabdomyolýza – kreatinkináza, myoglobin;
- Myokardiální postižení – troponin;
- Jaterní postižení – bilirubin, transaminázy, GMT;
- Zásadní parametry změn proteinového metabolismu, nefrotický syndrom – elektroforéza proteinů séra, free-lite, imunofixace;
- Sekundární hyperparathyreoidismus – parathormon, hypotyreóza – TSH;
- Pomocné posouzení anémie – Fe metabolismus, volný hemoglobin.
- Imunologická vyšetření podle zvažovaného typu postižení:
- Orgánově specifické – antiGBM (bazální membrána glomerulů);
- Orgánově nespecifické – ANCA (C-ANCA,P-ANCA) – proti cytoplasmě neutrofilů, antinukleární (ANA), proti extrahovatelným nukleárním antigenům (ENA), dsDNA a antinukleosomální, ASLO, kryoglobulin.
- CIK, C3,4, subpopulace lymfocytů.
Zobrazovací metody
Metodou první volby je vždy ultrazvukové vyšetření, které nasměruje v souhlase s klinickým obrazem další diagnostické zobrazovací a funkční metody a oborové řešení renální poruchy. Při sonografii je prioritní vyloučení subrenální blokády ledviny vyžadující akutní urologickou intervenci, ostatní stavy vyžadují péči internisty.
1. Ultrazvuk
- Morfologie ledvin, stav vývodných močových cest (blokády), retence v močovém měchýři, struktura prostaty, popř. dělohy;
- Prokrvení ledvin globálně, průkaz stenózy magistrálních tepen (rozhodující pro nasměrování dalšího potupu při podezření na akutní/chronický uzávěr), posouzení rezistence na úrovni středních a malých korových tepen, trombózy renálních žil;
- Sonografie umožní komplexní posouzení vztahu k ostatním abdominálním orgánům (zejména vyloučení aneurysmatu aorty se vztahem k aa. renales, cirhóze jater s portální hypertenzí, tumorů nadledvin, uzlinových syndromů, blokády ureterů gynekologickým tumorem, průkaz ascitu a hydrothoraxu).
2. RTG
- Nativní rentgenový snímek cílený na oblast retroperitonea provádíme s podezřením na přítomnost kontrastní lithiázy v oblasti ledvin a močovodu.
- Vylučovací urografii s použitím kontrastní látky podané intravenózně a následně vylučované ledvinou se provádí k posouzení uložení, funkce ledvin a také k průkazu lithiázy.
- CT angiografii ledvin volíme k průkazu stenózy renálních tepen při vyšetření renovaskulární hypertenze, při vyšetřování nádorů ledvin, zřídka k průkazu a lokalizaci blokády ureterů. CT břicha většinou specifikuje předchozí ultrazvukový nález, doplňuje klíčovou informaci o vztahu k okolním strukturám, orientačně k vylučovací funkci ledvin. CT-angiografii indikujeme při důvodném podezření na stenózu magistrálních renálních tepen. Pro intervenci na renálních tepnách se volí přímá angiografie.
- Denzitometrie – metota používaná k detekci kostní hustoty v následné diagnostice renální osteopatie.
3. Magnetická rezonance ledvin
Je alternativou vyšetření CT ve stejných indikacích včetně cévních (MR-angiografie renálních tepen).
Intravenózní podání rtg i MR kontrastní látky je nutno pečlivě zvažovat u pacientů s údajem o snížené glomerulární filtraci, zejména u diabetiků, pacientů po chemoterapii, starých a dehydratovaných. Lékař indikující vyšetření se přitom řídí zejména hodnotou kreatinémie, údajem o diuréze. V přípravě před vyšetřením je obecně nutné zejména kvalitní zavodnění pacienta a zachovalá dobrá diuréza (min. 2500ml/d), jako nefroprotektivum lze doporučit podání během 24 až 48 hodin před a po vyšetření infúzně N-acetylcystein v dávce 300mg/den.
4. Izotopové metody
Izotopové metody slouží k posouzení izolované funkce ledvin, k posouzení drenáže nebo ložiskových změn.
Lze použít:
- Vyšetření statickou scintigrafií ledvin – velikost a tvar ledviny, stranový podíl (%) na funkci, ložiskové změny;
- Dynamickou scintigrafii ledvin – posouzení funkční zdatnosti (%) ledvin a drenáže (významnost a lokalizace obstrukce);
PET/CT je metodou diagnostiky tumorů nejasné lokalizace a nejasných zánětlivých procesů. Specificky pro nádory ledvin se však většinou nepoužívá, protože akumulace fluorodeoxyglukózy je v renálních tumorech variabilní a dostačující je CT vyšetření.
Další metody
- Cystoskopie – endoskopické vyšetření ke stranové lokalizaci zdroje makroskopické hematurie, útvary v močovém měchýři, intervence ke zprůchodnění ureterální blokády;
- Biopsie ledvin – k histologickému vyšetření při systémových onemocněních, přesné specifikaci zánětlivých změn ledvin, diagnostika rejekce (odvržení) transplantované ledviny;
- Kostní biopsie (trepanobiopsie) – k bližšímu určení typu kostního postižení při renální osteopatii;
- Echokardiografie – metoda umožňující posílit či zpochybnit diagnostiku kardiovaskulárního postižení při onemocnění ledvin a posílit indikaci jiných vyšetření a léčebných postupů ve vztahu k ledvinám (etiologie renovaskulární hypertenze, df. dg. srdečního selhání, diagnostika uremické kardiomyopatie, perikarditidy, postižení chlopní, průkaz pohrudničního výpotku);
- EKG – v rámci komplexnosti diagnostiky: koexistence s ischemickou chorobou srdeční, známky hypertrofie levé komory, arytmie, známky hyperkalémie.
- Nativní RTG hrudních orgánů patří ke standardním vyšetřovacím metodám, ve vztahu k ledvinám jde zejména o posouzení převodnění, pohrudničních výpotků, zvětšení srdce, postižení plic při současném zánětu ledvin u některých typů onemocnění.
Klasifikace poruch renálních funkcí
V praxi se používá klasifikace RIFLE zahrnující kategorii akutní poškození ledvin (AKI, acute kidney injury). Je uvedena v následující tabulce.
| Tabulka 4. Kritéria RIFLE a stádia akutního poškození ledvin (AKI) podle nové klasifikace |
| RIFLE |
SKr Kreatinin v séru (µmol/l) |
Glomerulární filtrace GF (ml/s) |
Diuréza D (ml/hod) |
Stádia AKI |
| Riziko (Risc) |
SKr zvýšený o 50 % (tj. 1,5x) |
GF pokles o 25 % v průběhu 1 – 7 dní |
Oligurie D < 0,5 ml/kg/hod minimálně 6 hodin
Neoligurie – diuréza zachována
|
I. stádium |
| Poškození ledvin (Injury) |
SKr zvýšený o 100 % (tj. 2x) |
GF < o 50 % |
Oligurie D < 0,5 ml/kg/hod minimálně 12 hodin
Neoligurie – diuréza zachována
|
II. stádium |
| Selhání ledvin (Failure) |
SKr zvýšený o 200 % (tj. 3x), nebo vzestup na > 350 µmol/l |
GF < o 75 % |
Oligurie D < 0,5 ml/kg/hod delší než 24 hodin anebo anurie minimálně 12 hodin
Neoligurie – diuréza zachována
|
III. stádium |
| Ztráta funkce ledvin (Loss) |
Akutní selhání ledvin
Akutní selhání ledvin s afunkcí trvající déle než 4 týdny
|
|
Oligurie nebo anurie |
|
| Terminální ztráta funkce ledvin (End-stage kidney disease) |
Akutní selhání ledvin s afunkcí trvající déle než 3 měsíce |
Pro obtížnost přesného měření glomerulární filtrace jsou v laboratorní diagnostice akutního selhání/poškození ledvin používány hodnoty sérového kreatininu a diurézy.
Při klasifikaci chronického selhání ledvin se používá schéma K/DOQI.
| Tabulka 5. Nově navržená klasifikace chronického onemocnění ledvin |
| Stadium. |
Popis. |
Glomerulární filtrace (GF) [ml/s/1,73m2] |
| 1 |
Poškození ledvin s normální funkcí |
Kalkulovaná GF > 5. percentil zdravých osob |
| 2 |
Poškození ledvin se sníženou funkcí ledvin a rezervou
Bez klinických známek funkční nedostatečnosti
|
Kalkulovaná GF < 5. percentil zdravých osob, ale GF >0,5 |
| 3 |
Poškození ledvin s nedostatečnou funkcí ledvin (chronické selhání ledvin) |
GF = 0,25 – 0,49 |
| 4 |
Těžké poškození ledvin s život ohrožující nedostatečností funkce ledvin |
GF < 0,25 |
| 5 |
Pokročilá/úplná destrukce ledvin |
Závislost na dialýze |
Léčba
Léčba je vedena na několika úrovních:
- Obecně renální – léčba již rozvinutého/hrozícího renálního selhávání a selhání, renoprotektivní léčba a metabolická podpora
- Korekce poruchy vnitřního prostředí –zejména v oblasti minerálního,vodního hospodářství a acidobázie
- Léčba specifického onemocnění s postižením ledvin
1. Léčba akutního oligoanurického selhání ledvin
Oběhová stabilizace směřující k úpravě perfúze ledvin (při prerenáulním selhání nebo v polyurické fázi akutního renálního selhání):
- Úpravou hypotenze (podpora sympatomimetiky – dopaminem, včetně beta-dávky a noradrenalinem jen po nezbytně nutnou dobu, cílový systolický tlak minimálně 100 – 110 mm Hg)
- Doplněním cirkulujícího volumu, důležité je monitorování centrálního žilního tlaku, docílení normotenze.
- Preventivní podání Ca2+ antagonistů (indikována non-dihydropyridinová léčiva- amlodipin, diltiazem), pokud to stav dovoluje.
Úprava vodního a iontového hospodářství s navozením diurézy.
Forsírovaná diuréza probíhá za předpokladu dostatečného doplnění cirkulujícího volumu:
- Optimální je zavedení centrálního žilního katetru s monitorováním centrálního žilního tlaku a monitorováním diurézy permanentním močovým katetrem s velkou objemovou náloží krystaloidů – tzv. volumexpanze (výběr krystaloidů podle aktuálního iontogramu Na, K, Cl, Ca, P a ABR). Diuréza je navozena, resp. forsírována vysokou dávkou kličkových diuretik (furosemid 10 – 30 mg/hod) v kontinuální infúzi injektomatem. Cílem je dosáhnout obnovení diurézy, při oligoanurii na 100 – 200ml/hod a více. Tento způsob je určen zejména pro řešení prerenální příčiny při dehydratacích, toxickém poškození ledvin a tam, kde nedominují kardiovaskulární projevy z převodnění. Paralelně podporujeme vysoký příjem tekutin p.o.
- Při nemožnosti a vyčerpání metody forsírované diurézy (během několikadenního trvání) je další souběžnou metodou volby hemodialýza, při níž forsírovaná diuréza pokračuje. Je vhodné ji indikovat i jako vstupní eliminační metodu při extrémně vysokých hodnotách dusíkatých katabolitů, v terminální fázi ledvinné poruchy bez perspektivy návratu/zlepšení diurézy, při neupravující se hyperkalémii (K+ > 6,5 mmol/l) anebo komplexní renální poruše (vysoké N katabolity, převodnění, hyperkalémie, těžká acidóza, laktacidémie, oligoanurie). Hemodialýza je metodou prvé volby u řady intoxikací.
Korekce metabolické acidózy:
- Použijeme klasický přístup konzervativní léčbou NaHCO3 4,2% (resp. 8,4%, který slouží ke korekci zejména do úrovně pH 7,25 – 7,30), vstupně se zřejmým vysokým deficitem bikarbonátů (BE – 5-10 mmol/l) (obr. 3). Opatrné podávání je nutné zejména u extrarenálních příčin acidózy, kde po rehydrataci a se zlepšením prokrvení ledvin tyto rychle převezmou další úpravu a dalším podáním (např. při pH 7,30) hrozí iatrogenně navozený nebezpečný rychlý přechod do alkalózy.
- Současně nutno s úpravou acidózy korigovat kalémii,resp. respektovat redistribuci kalia v rámci posunu pH (tabulka 6).
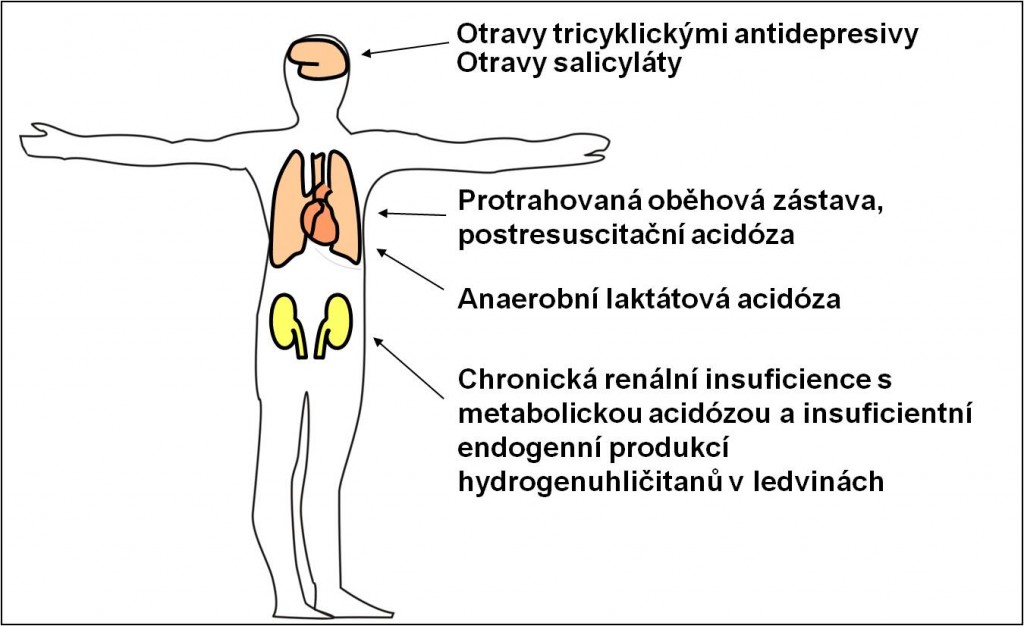 [3]
[3]Obr. 3. Ilustrace indikací podávání hydrogenuhličitanů při acidobazických poruchách, které doplňují přísné pravidlo o podávání hydrogenuhličitanů jen při jejich přímých ztrátách.
| pH |
Normální hodnoty K+ (mmol/l) |
| 6,8 |
6,5 – 8,0 |
| 7,1 |
5,5 – 6,5 |
| 7,3 |
5,2 |
| 7,4 |
4,5 |
| 7,7 |
3,5 |
Tabulka 6. Normální (redefinované normální) hodnoty koncentrace K+ v séru při acidémii.
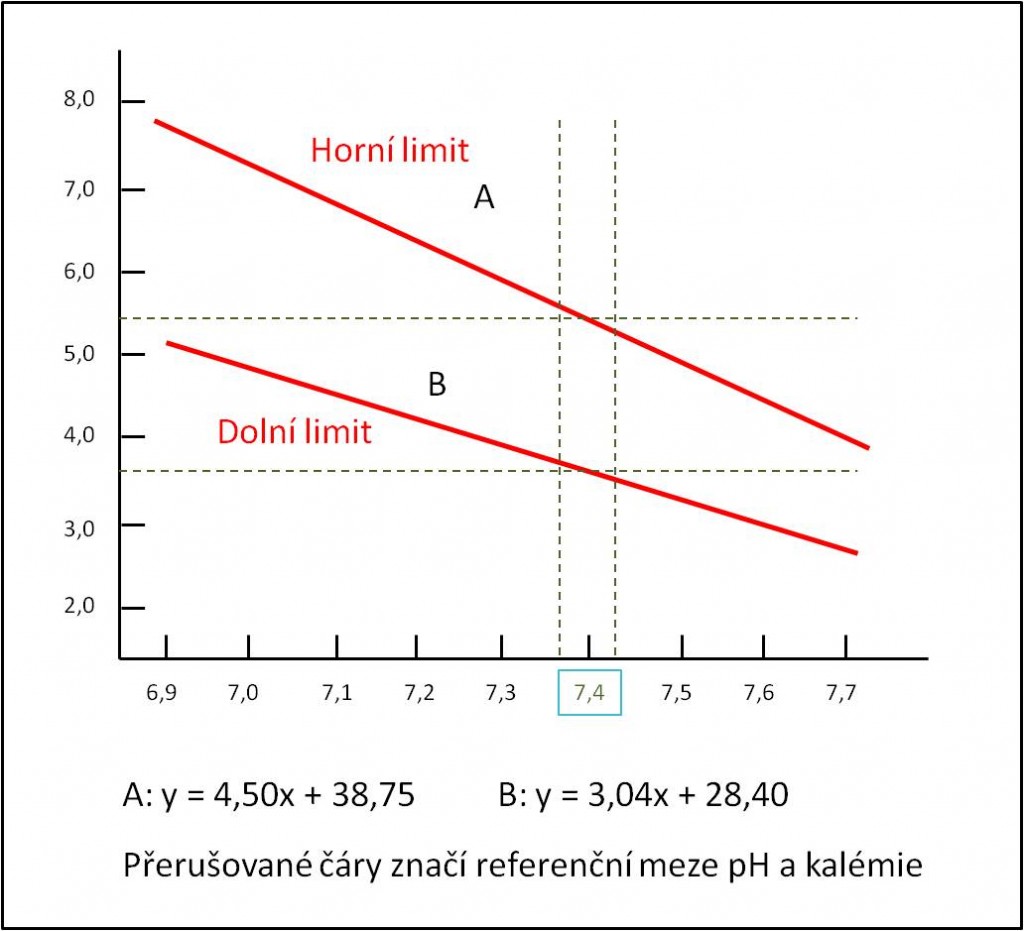 [4]
[4]Obr. 4. Vztah referenčních hodnot kalémie k hodnotám pH plazmy
Korekce hyperkalémie:
Není nutno upravovat hyperkalémii, která je prosta klinických projevů a odpovídá stupni acidózy (podání NaHCO3, dialýza), ani u nesymptomatických pacientů dlouhodobě navyklých na chronickou hyperkalémií. Zde volíme monitorování. U těžké acidózy s kritickou hyperkalémií (uvádí se nad 6.2 – 6.5 mmol/l), zejména u otrav nebo u těžké laktátové acidózy, je dialýza metodou prvé volby.
V ostatních případech lze zvolit pomalejší úpravu:
- Forsírovaná diuréza navodí vedle natriurézy i kaliurézu
- Metabolizace v buňkách pomocí infúzí glukózy s inzulínem v rámci rehydratace anebo metabolické podpory
- Použití iontoměniče Calcium resonium (2 odměrky každé 2 – 3 hodiny) – velmi účinný prostředek
- Zastavujeme jakýkoli přívod kalia v potravě (ovocné kompoty, brambory, zelenina), kalium šetřící diuretika, ACEi
- Inhibice účinku na buněčné membráně – podání vápníku (bolusově Calcium gluconicum); bradykardii lze ovlivnit betamimetiky, atropinem.
2. Léčba pokračujícího, chronického selhání ledvin s dopadem na vnitřní prostředí
Po zvládnutí akutního selhání ledvin s navozením diurézy anebo paralelně s nutně probíhající dialýzační léčbou (zejména u pacientů s perspektivou alespoň částečné obnovy renálních funkcí), vedeme léčbu nefroprotektivní, resp. pokračujeme standardní léčbou chronického ledvinného selhávání v oblasti úprav vnitřního prostředí:
- dieta, navození a monitorování natriurézy, kaliurie a vodní diuréy, korekce proteinurie, acidózy
- léčba směřovaná na eliminaci patologií Ca-P metabolismu
- intervence metabolických rizikových faktorů (obezita, poruchy glykoregulace, lipidů, kouření)
- léčba směřovaná na normalizaci poruchy hematopoezy
- souběžně běží orgánově směrovaná léčba poruch kardiovaskulárních, již vzniklých komplikací v oblasti endokrinní – zejména léčba hypertenze, depistáž manifestací a hrozících klinicky významných projevů aterosklerózy (ICHDK, CMP, ICHS) a uremické kardiomyopatie, eliminace hyperparathyroidismu (extirpace adenomů a farmakoterapie u inoperabilních).
1. Ledvinová dieta
- denní příjem bílkovin 0,8 g /kg tělesné hmotnosti, při poklesu GF dle MDRD pod 0.66 ml/min pak 0,6 g/kg tělesné hmotnosti
- omezení cukrů, tuků v dietě, redukce nadváhy, nekouření (aktivuje systém RAAS)
- podle tendence k hyperkalémii omezujeme přísun kalia v dietě (čerstvé brambory, ovoce, zelenina)
- bilance tekutin se odvíjí od stupně zachovalé diuretické odpovědi; doporučuje se bilance příjem = diuréza + 500 ml
- podávání kličkových diuretik v případě nedostatečně navozené diurézy při dostatečném příjmu tekutin
- pokračování korekce acidózy podáváním tablet bikarbonátu
- proteinurii snížit podáním ACEi, popř. AT1R antagonistů, pečlivou léčbou na hodnoty normotenze u hypertoniků (120/80 -130/80 mm Hg)
2. Při sekundárním hyperpatathyreoidismu
Je doporučena nízkobílkovinná dieta 0.8 g/kg tělesné hmotnosti s důrazem na omezení mléčných výrobků. Podáváme tzv. vazače fosfátů ve střevě – částečně se vstřebávající kalcium carbonicum (CaCO3) anebo nověji neresorbovatelné polymery (sevelamer). Současně je substituován vitamín D ve formě aktivního metabolitu (kalcitriol).
Účinným léčebným přístupem rezistentní hyperparathyreózy je parathyroidectomie, kterou lze kombinovat s autotransplantací jednoho z tělísek podkožně (na předloktí), u inoperabilních léčba cinalkacetem (senzitizér receptorů na povrchu hlavních buněk příštítných tělísek pro kalcium na extracelulární kalcium, čímž je docíleno snížení stimulace sekrece PTH).
3. Při CHSL
Podáváme ketoanaloga essenciálních aminokyselin, snažíme se o vyrovnanou bílkovinnou bilanci s předcházením malnutrici
4. Korekce anémie
Fe preparáty, vitamin B12, kys. listová, popř. erytropoetin
5. Zlepšení intrarenální cirkulace
Preferovat antihypertenziva typu non-dihydropyridinových Ca antagonistů, sympatolytik.
Při prevenci a léčbě proteinurie otestovat efekt ACEi/AT1 . Při antihypertenzní léčbě pečlivě monitorujeme možný nežádoucí efekt léčby ACEi na hladinu kalia a kreatinémii.
Zpracoval: Rudolf Metelka, III. interní klinika LF UP a FN v Olomouci. Formální úpravy: Jaroslav Veselý, Ústav patologické fyziologie LF UP v Olomouci.
Article printed from Tvorba a ověření e-learningového prostředí pro integraci výuky preklinických a klinických předmětů na LF a FZV UP Olomouc: http://pfyziolklin.upol.cz



