Téma: Fyziologie a patofyziologie vzájemných přeměn živin
Posted By 0003 On 27.3.2012 @ 7:55 In 7.1. Komplexní (civilizační) metabolické poruchy | Comments Disabled
Charakteristika
Energetická potřeba organismu se kryje hlavními živinami – sacharidy, lipidy a proteiny. Kromě dostatečné energetické hodnoty je nutno dbát na kvalitativní hlediska stravy.
Kvalitativní hlediska
- Vzájemný poměr hlavních živin;
- Zastoupení esenciálních složek hlavních živin (esenciální aminokyseliny, esenciální mastné kyseliny atd.);
- Příjem vody a minerálů;
- Obsah esenciálních složek (vláknina), vitamínů, antioxidantů, mikroelementů;
- Nízký obsah škodlivých složek (sůl, trans-nenasycené mastné kyseliny aj.).
Sacharidy a proteiny obvykle představují méně než 25 % hmotnosti potravin. Výjimkou jsou umělé koncentráty, např. cukr. Tuk je unikátní potravina. Přijaté množství tuku obvykle představuje 100 % lipidů.
Sacharidy a tuk jsou složky šetřící proteiny. Pokud je jich ve stravě dostatek, pokrývají energetické potřeby a proteiny se pro získání energie prakticky nevyužívají.
Příjem proteinů
Je nutný přísun plnohodnotných proteinů. Doporučená dávka proteinů je kolem 50 g/den, u dětí více. Podrobněji:
Pro 70kg muže je doporučená dávka:
- 56 g proteinů/den, tj.
- 0,8 g proteinů/kg tělesné hmotnosti/den, neboli
- 9 g N/den.
- Denní dávka proteinů pokrývá asi 960 kJ/den (230 kcal/den).
Pro 56kg ženu je doporučená dávka:
- 44 g proteinů/den, tj.
- asi 0,8 g proteinů/kg tělesné hmotnosti/den, neboli
- 7 g N/den.
- Denní dávka proteinů pokrývá asi 755 kJ/den (180 kcal/den)
Denní potřeba proteinů u dětí je vyšší než u dospělých:
- Prvních 6 měsíců života:
- Asi 2,2 g proteinů/kg tělesné hmotnosti/den.
- Děti ve věku 6 měsíců – 1 rok:
- Asi 1,6 g proteinů/kg tělesné hmotnosti/den.
- Děti ve věku 1 – 3 roky:
- 1,2 g proteinů/kg tělesné hmotnosti/den.
Podobnou nebo vyšší potřebu mají nemocní s chirurgickými traumaty, popáleninami, anebo infekcemi,
Plnohodnotné a neplnohodnotné proteiny
Živočišné proteiny obvykle jsou plnohodnotnými proteiny. Rostlinné proteiny mohou být neplnohodnotnými (parciálními) proteiny – neobsahují potřebné esenciální aminokyseliny.
Obilní zrna a zrna kukuřice např. neobsahují téměř žádný tryptofan. Pokud tvoří převážnou složku stravy (zejména v Afrických zemích), prakticky jde o stravu s nedostatkem proteinů, protože využitelnost aminokyselin pro proteosyntetické pochody určuje ta aminokyselina, která je ve stravě zastoupena nejméně. Jedinci převážně konzumující tuto stravu (zejména děti) trpí syndromem zvaným kwashiorkor (téma Patofyziologie podvýživy, hladovění a poruch příjmu potravy [1]).
Normální koncentrace volných aminokyselin v cirkulaci je asi 3 – 5 mmol/l; to je průměrně 150 – 250 μmol/l na jednu aminokyselinu. Aminokyseliny ale nejsou zastoupeny rovnoměrně. Nehojnější aminokyselinou v plazmě je glutamin. Normální poměr koncentrací větvených aminokyselin ke koncentracím aromatických je mezi 1,4 – 2,0. Játra jsou odpovědná jak za udržování stálé koncentrace aminokyselin v plazmě, tak za jejich poměrné zastoupení (téma jaterní encefalopatie – Patofyziologie poškození a selhání jater [2]).
Příjem sacharidů
Sacharidy jsou hlavní složkou naší diety pokrývající denní energetický příjem. Kryjeme jimi nejméně 55 % celkového příjmu energie. Přijímáme je jako jednoduché anebo složené sacharidy.
Hlavním sacharidem v plazmě je glukóza (3,5 – 5,6 mmol/l). Za udržování stálé koncentrace glukózy v plazmě jsou jako výkonný orgán pod hormonální a nervovou regulací odpovědná játra (téma Patofyziologie a klinická fyziologie diabetes mellitus [3]).
Příjem lipidů
Zastoupení tuků v dietě by nemělo převyšovat hranici 30 % celkového energetického příjmu. Ve stravě také mají význam pro vstřebávání vitamínů.
Nasycené mastné kyseliny převážně jsou živočišného původu. Nenasycené mastné kyseliny většinou jsou rostlinného původu a jsou také hojně zastoupeny v rybím oleji. Jsou mezi nimi i esenciální mastné kyseliny (kys. olejová, linolová, linolenová aj.). Mají četné jiné funkce než energetické.
Trans-izomery nenasycených mastných kyselin se v přirozené stravě vyskytují v minimálním množství. Vznikají průmyslovým ztužováním olejů. Mají vážné zdraví nebezpečné účinky. Jejich množství v potravinách musí být kontrolováno a ve vyspělých zemích je přísně limitováno normami.
Koncentrace volných mastných kyselin v krevní plazmě je v klidu 0,5 – 1 mmol/l. Odpovídá to obsahu 0,5 g mastných kyselin v celé cirkulaci. Při hladovění nebo diabetu může být koncentrace mastných kyselin v plazmě až 5 – 8krát vyšší.
Molekuly triacylglyceridů, fosfolipidů a cholesterolu jsou transportovány v oběhu ve formě lipoproteinů. Naproti tomu volné, neesterifikované mastné kyseliny, jsou transportovány hlavně vázány na albumin. Normální poměr navázaných mastných kyselin (MK) je 3 molekuly MK/1 molekulu albuminu; poměr může být mnohem vyšší. Poločas obměny mastných kyselin v plazmě je velice krátký – pouhé 2 – 3 minuty.
Vláknina
V dietě je obsažena ve dvou formách. Ve vodě rozpustná vláknina zahrnuje pektin, gumy a slizy. Ve vodě nerozpustná vláknina zahrnuje celulózu, lignin a hemicelulózu. Doporučená denní dávka vlákniny je 20 – 35 g.
Funkce vlákniny jsou různorodé:
- Váže větší množství vody ve střevě a zvětšuje náplň střeva;
- Zvětšuje biomasu střevního lumen, protože je hlavním živným zdrojem pro bakteriální flóru;
- Zvětšený intraluminální obsah stimuluje peristaltiku;
- Usnadňuje a urychluje posun střevního obsahu;
- Zabraňuje zácpě;
- Zmírňuje průjem;
- Pomáhá při hubnutí (pocit nasycení);
- Snižuje hladinu cholesterolu;
- Omezuje tvorbu žlučových kamenů;
- Snižuje riziko rakoviny tlustého střeva a konečníku;
- Snižuje riziko tvorby hemoroidů.
Vzájemné přeměny živin
Přeměna sacharidů na tuk
Zvýšení hladiny inzulínu, k němuž dochází po jídle (postprandiálně), zajišťuje clearance zvýšené plazmatické glukózy přepnutím metabolismu z oxidace mastných kyselin na oxidaci sacharidů a následné pokrytí všech energetických potřeb ze sacharidových zdrojů. Respirační kvocient dosahuje bezprostředně po jídle hodnoty 1,0 a vrací se k hodnotám mezi 0,8 – 0,9 (obnovuje se oxidace tuku) až asi za 8 – 10 hodin po jídle. Tyto změny jasně ukazují, že dosažení rovnováhy sacharidů má přednost před dosažením rovnováhy lipidů. Děje se to následujícími hlavními mechanismy:
- Zvýšeným transportem glukózy do inzulín-senzitivních tkání;
- Zvýšenou oxidaci glukózy v inzulín-senzitivních tkáních;
- Zástavou glukoneogeneze, ukládáním glukózy ve formě glykogenu.
Kapacita k přeměně sacharidů v lipidy v lidských játrech je omezená a v tukové tkáni minimální. Sacharidy se mění na lipidy ve stavu nalačno asi z 1 % a postprandiálně asi ze 2 %. Absolutní produkce lipidů de novo ze sacharidů v játrech se odhaduje na jen asi 5 g mastných kyselin/den (necelé 2 kg/rok). Dokonce i při dietě s vysokým obsahem sacharidů a nízkým obsahem lipidů dosahuje produkce mastných kyselin de novo jen asi 12 g/den (necelých 5 kg/rok).
Sacharidy, přesněji určité jejich metabolity, mohu být transaminovány na neesenciální aminokyseliny. Nemohou nahradit přísun proteinů. jejich dostatečný přívod však má proteiny-šetřící efekt, protože jinak by se proteiny musely mobilizovat pro zajištění glukoneogenezy.
Přeměna proteinů na sacharidy
Podobně jako rovnováha sacharidů se i rovnováha proteinů (dusíku, N) při změnách příjmu proteinů obnoví v průběhu nanejvýš několika dnů. Nadbytek dodaných aminokyselin se oxiduje a dusík se vylučuje jako močovina. Hmotnost tělesných proteinů se dlouhodobě udržuje na konstantní výši, pokud:
- Je pokryta minimální denní potřeba N;
- Nedochází ke stimulaci svalové hmotnosti fyzickou aktivitou.
Při nedostatečném přívodu sacharidů se proteiny masivně mobilizují pro zajištění glukoneogeneze.
K lipogeneze de novo z proteinů dochází v lidském těle stejně jako ze sacharidů jen v malé míře.
Regulace rovnováhy lipidů
Oxidace lipidů důležitým zdrojem energie jak pro glukoneogenezu, tak pro proteosyntézu. Navzdory tomu ze složek lipidů může sloužit jako prekurzor glukoneogenezy pouze glycerol. Sacharidy se nemohou tvořit z mastných kyselin. Stejně tak se nemohou z lipidů syntetizovat proteiny. Jedinou aminokyselinou, která může vznikat transmaminací produktů oxidace mastných kyselin, je glycin. Z glycerolu může nepřímo vznikat alanin.
Výsledkem postprandiálního zvýšení hladiny inzulínu je tuk-šetřící účinek sacharidů. Jsou za to odpovědné následující mechanismy:
- Inhibice lipolýzy (inhibice hormon-senzitivní/katecholamin-senzitivní lipázy v adipocytech) a inhibice uvolňování mastných kyselin z adipocytů;
- Stimulace syntézy triacylglyceridů v játrech a jejich re-export;
- Stimulace transportu mastných kyselin (aktivací lipoproteinové lipázy na povrchu endotelií) do adipocytů a zvýšené ukládání triacylglyceridů v adipocytech;
- Nedochází ke stimulaci, nýbrž k útlumu oxidace lipidů, na rozdíl od zvýšené oxidace sacharidů nebo aminokyselin.
Kontrola rovnovážné bilance lipidů výrazně zaostává za regulací rovnovážné bilance sacharidů a proteinů. Rovnováhy lipidů v těle se na rozdíl od rovnováhy sacharidů a aminokyselin nedosahuje v měřítku hodin nebo dnů. Clearanci („odklízení“) lipidů z plazmy zajišťuje ukládání lipidů do tukové tkáně. Hlavně jde o syntetické, nikoliv oxidační pochody. Na clearanci lipidů se významně podílí re-export lipidů z jater ve formě VLDL. Složení zásobních lipidů a složení lipidů v játrech významně koreluje se složením lipidů v potravě. Triacylglyceridy se v tukové tkáni kompletně obmění za 2 – 3 týdny, tedy rychleji než 1krát za měsíc.
Výsledkem chronické pozitivní lipidové bilance je hromadění lipidů v těle. Zásoby lipidů jsou 50 – 100krát větší než zásoby glykogenu. Není mechanismus, který by dokázal odbourat tukovou tkáň za 1 – 2 dny, jako se to děje v případě glykogenu. Lipidy jsou v adipocytech obsaženy v tekutém stavu. Pouze tekuté lipidy mohou být štěpeny a mobilizovány. Pokud je tkáň dlouhodobě vystavena chladu, lipidy se v průběhu několika týdnů obohacují o kratší anebo o nenasycené mastné kyseliny, které mají nižší body tání.
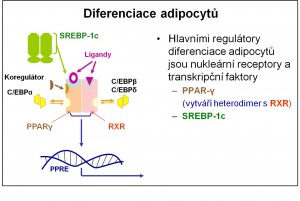
Diferenciace adipocytů
Adipocyty se netvoří jen v raném dětství, nýbrž se diferencují z pre-adipocytů (buněk podobných fibroblastům) v kterékoliv fázi života. Diferenciace je řízena hlavně receptory aktivátorů proliferace peroxisomů (PPAR) spolu s dalšími jadernými receptory a transkripčními faktory. Tuková tkáň plní v organismu četné prospěšné a nenahraditelné funkce. Nadměrné hromadění lipidů v adipocytech však vede k obezitě. Pozdější hromadění lipidů v tuku prostých tkáních vede k lipotoxicitě.
Obr. 1. Schéma základní regulace diferenciace adipocytů.
Zpracoval: Jaroslav Veselý, Ústav patofyziologie LF UP
Article printed from Tvorba a ověření e-learningového prostředí pro integraci výuky preklinických a klinických předmětů na LF a FZV UP Olomouc: http://pfyziolklin.upol.cz
URL to article: http://pfyziolklin.upol.cz/?p=3361
URLs in this post:
[1] Patofyziologie podvýživy, hladovění a poruch příjmu potravy: http://pfyziolklin.upol.cz/?p=3222
[2] Patofyziologie poškození a selhání jater: http://pfyziolklin.upol.cz/?p=3460
[3] Patofyziologie a klinická fyziologie diabetes mellitus: http://pfyziolklin.upol.cz/?p=6887
[4] Image: http://pfyziolklin.upol.cz/wp-content/uploads/2012/01/DifAdipoc.jpg
Click here to print.