Úvod
Akutní myeloidní leukémie (AML) jsou heterogenní skupinou maligních onemocnění krvetvorné tkáně, charakterizované hromaděním abnormálních nezralých buněk (blastů) a porušenou tvorbou normálních buněk krvetvorby. Vznikají maligní transformací kmenové hematopoetické buňky, která se v případě AML diferencuje v myeloidní, myelomonocytární, méně často v erytroidní či megakaryocytární blasty.
Epidemiologie
AML tvoří 80% akutních leukémií u dospělých a 15-20% u dětí. Jejich výskyt narůstá s věkem, nejčastěji postihuje jedince nad 60 let (medián věku nemocných je 65-70 let). Průměrný výskyt nových případů AML je v celé populaci je 3,4/100 000 obyvatel, v populaci starší 65 let dosahuje hodnoty 15/100 000 obyvatel. Ročně ve světě onemocní přibližně 300 000 osob.
Etiologie a patogeneze
Příčina vzniku onemocnění není známa, jsou však známy některé faktory spojené s vyšším rizikem výskytu AML. Jako riziková se uvádí expozice některým chemickým látkám – zejména benzenu. Častěji se onemocnění vyvíjí u nemocných s některými vrozenými chromozomovými poruchami (např. Downův syndrom nebo Bloomův syndrom). U cca 20% nemocných je příčinou předešlá cytotoxická léčba (cytostatika – alkylační látky, inhibitory topoizomerázy II, radioterapie) nebo se AML vyvíjí z jiného hematologického onemocnění – myelodysplastického syndromu (MDS) či myeloproliferativních nemocí (MPN) – v těchto případech se leukémie označuje jako sekundární.
Podstatou AML je nádorová přeměna kmenové hematopoetické buňky, která je spojená s úplnou nebo částečnou ztrátou schopnosti vyzráváni ve funkční elementy krve při zachovalé schopnosti jejich dalšího množení. Vyzrávání postižené krvetvorné buňky, ze které se u zdravého člověka vyvíjí různé druhy bílých krvinek, ale také erytrocyty a trombocyty, se zastaví na úrovni blastů. Jejich následné nekontrolované množení a delší přežívání (pro narušenou apoptózu) pak vedou ke kumulaci těchto nádorových buněk v organismu, zejména v kostní dřeni a krvi. Leukemické buňky jsou funkčně neplnohodnotné, nejsou tedy schopné plnit své původní fyziologické funkce. Navíc jejich kumulace v kostní dřeni vede k útlaku fyziologické krvetvorby a z toho plynoucím projevům onemocnění. Vývoj onemocnění je velice rychlý. Od prvých nenápadných příznaků do vzniku výrazných potíží, kdy již nemoc neunikne diagnóze, uplyne obvykle jen několik málo týdnů. Celkový počet leukemických buněk dosahuje ve stadiu rozvinuté choroby 1×1012, což si lze představit jako solidní nádor o průměru téměř 15 cm.
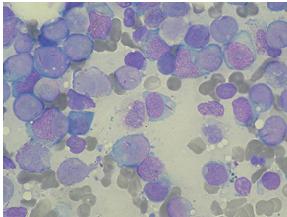
Obr. č. 1. (vlevo) Kostní dřeň zdravého člověka (autor: Bob Jagalindo, www.wikipedia.org)
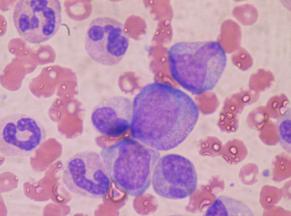
Obr. č. 2. (vpravo) Kostní dřeň pacienta s AML (autor: Paulo Henrique Orlandi Mourao, www.wikipedia.org)
Hlavní příznaky
Příznaky u pacientů s AML jsou nespecifické a značně pestré. Většina nemocných přichází k lékaři s tzv. chřipkovými příznaky, k nimž patří únava, nechutenství, ztráta hmotnosti a zvýšení tělesné teploty. Často se však těmto příznakům nevěnuje dostatek pozornosti a jejich příčina se přikládá zvýšené fyzické či psychické zátěži, k pomyšlení na leukémii vede pak až vyšetření krve. Další klinické příznaky jsou pak způsobené nedostatkem funkčních krvinek v cirkulaci - cytopenie. Nedostatek červených krvinek – anémie se projevuje únavou, malátností, rychlou unavitelností při námaze, bušením srdce a bledostí kůže a sliznic. Při granulocytopenii mají pacienti často infekce, např. dýchacích a močových cest. Tyto infekce nereagují dostatečně na antibiotickou léčbu a často se opakují. Dalším projevem AML může být krvácení, které je způsobeno nedostatkem krevních destiček – trombocytopenie. To se může projevit jako dlouhotrvající krvácení z nosu, dásní, krvácení do kůže (petechie) nebo výrazné gynekologické krvácení a podobně. Přítomny mohou být také neurologické příznaky (při průniku blastů do centrálního nervového systému), tato komplikace se však vyskytuje u méně než 5% pacientů. K relativně vzácným příznakům patří také infiltrace dásní či kůže leukemickými buňkami (především u monocytárních a myelomonocytárních AML). Velký počet blastů v krvi může způsobit obtížný průchod krve malými cévami – syndrom leukostázy, což se projeví poruchami dýchaní (dyspnoe), bolestmi hlavy, bolestí na hrudi či poruchami vědomí, nebo také poruchami zraku. U akutní promyelocytární leukémie (APL) je dominujícím příznakem krvácení, způsobené poruchou koagulace vyvolanou působky uvolňovanými z nádorových buněk. Krvácení může být i život ohrožující – APL je z tohoto důvodu urgentním stavem v hematologii.
Obr. č. 3. (vlevo) Infiltrace dásní leukemickými buňkami (autoři: Herbert L. Fred, MD a Hendrik A. van Dijk, www.wikipedia.org)
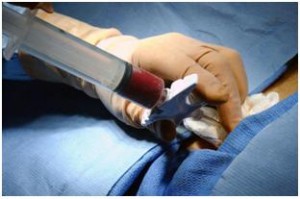
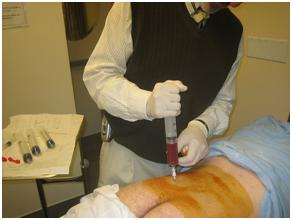
Obr. č. 4. (vpravo) Sternální punkce k odběru kostní dřeně (autor: Chad Mc Neeley, www.wikipedia.org)
Vyšetření a diagnóza
K lékaři obvykle nemocného přivedou některé z výše uvedených obtíží. Základním vyšetřením při podezření na AML je vyšetření krevního obrazu. V odebraném vzorku krve se hodnotí základní parametry – počet bílých krvinek, krevních destiček, množství hemoglobinu. Většina nemocných má v krevním obraze izolovanou leukocytózu (jen výjimečně přesahující 100×109/l), anémii nebo trombocytopenii, popřípadě jejich různé kombinace. Vždy se provádí optický rozpočet bílých krvinek, ve kterém u většiny nemocných nalézáme blasty a reziduální zralé granulocyty. Pro AML je charakteristické chybění středních vývojových stadií granulocytů (promyelocyty, myelocyty a metamyelocyty). Tento stav se označuje jako tzv. hilus leucaemicus.
Rozhodující pro stanovení diagnózy je vždy vyšetření kostní dřeně s nálezem více než 20% blastů ze všech jaderných buněk. Odběr kostní dřeně se provádí obvykle z hrudní kosti, tzv. sternální punkce, v místním znecitlivění. Vzorek dřeně je pak ještě podroben speciálním vyšetřením –imunofenotypizačním, cytogenetickým a molekulárně-genetickým, které slouží k přesnému určení typu AML. Imunofenotypizace stanovuje specifické antigenní markery na povrchu či v cytoplazmě blastických buněk a cytogenetika hodnotí změny v buňkách na úrovni chromozomů. Molekulární genetika se zabývá geny a jejich produkty. Výjimečně nemusí být splněna podmínka přítomnosti alespoň 20% blastických buněk v kostní dřeni. V případě nálezu cytogenetické změny specifické pro určitý subtyp akutní leukémie, např. t(8;21), lze diagnózu stanovit i při nižším procentuálním zastoupení blastických buněk.
Ukázka výsledku krevního obrazu pacienta s AML:
Upraveno podle: Szotkowski T, Faber E. Akutní leukemie. In: Faber E. et al. Základy hematologické diagnostiky 1. vyd. Olomouc, Univerzita Palackého v Olomouci, Lékařská fakulta, 2012; 153-159.
Diferenciální diagnostika
Z hlediska diferenciální diagnostiky je potřeba odlišit následující onemocnění a stavy:
- Leukemoidní reakce – reaktivní stav charakterizovaný zvýšenou produkcí granulocytů kostní dření pod vlivem růstových faktorů (G-CSF, GM-CSF) nebo vyplavením granulocytů z kostní dřeně do krve účinkem některých léků (glukokortikoidy, líthium). Charakteristickým znakem leukemoidní reakce je zvýšené zastoupení méně vyzrálých forem granulocytů v krvi, tzv. posun doleva. Na rozdíl od AML, které jsou způsobeny změnou genomu, je leukemoidní reakce výrazem velmi intenzívní stimulace granulocytopoezy pod vlivem faktorů uvedených výše – je tedy jen stavem přechodným, reaktivním.
- Myelodysplastický syndrom (MDS)
- Aplastická anémie
- Chronická myeloidní leukémie
- Karcinomatóza kostní dřeně
- Poškození kostní dřeně v souvislosti s léčbou
- Akutní lymfoblastická leukémie
Klasifikace
Klasifikace AML se vyvíjela od čistě morfologické a cytochemické charakteristiky myeloblastů z roku 1976, tzv. Francouzko-americko-britská klasifikace (FAB klasifikace).Pokroky v diagnostice na cytogenetické a molekulární úrovni, umožnily zavedení nové klasifikace AML, která daleko přesněji určuje jednotlivé typy leukémií a pomáhá při stratifikaci pacientů a výběru vhodné léčby. Nová WHO klasifikace AML byla do praxe zavedena v roce 2001 a zohledňuje již výsledky cytogenetického, molekulárně-biologického a také některé další ukazatele patogeneze nemoci (např. sekundární AML vzniklé v souvislosti s léčbou).
Tabulka č.1 : WHO klasifikace AML.
| AML s rekurentními genetickými abnormalitami |
| AML s t(8;21); RUNX1 – RUNX1T1 |
| AML s inv(16) nebo t(16;16); CBFB – MYH11 |
| APL s t(15;17); PML – RARA |
| AML s t(9;11); MLLT3-MLL |
| AML s t(6;9); DEK-NUP214 |
| AML s inv(3) nebo t(3;3); RPN1 – EVI1 |
| AML s t(1;22); RBM15 – MKL1 |
| AML s myelodysplastickými změnami |
| AML vzniklé v souvislosti s léčbou |
| AML blíže nespecifikované |
| AML bez diferenciace nebo s minimální diferenciací |
| AML bez maturace |
| AML s maturací |
| Akutní myelomonocytární leukémie |
| Akutní monoblastická a monocytární leukémie |
| Akutní erytroblastická leukémie |
| Akutní megakaryocytární leukémie |
| Akutní bazofilní leukémie |
| Akutní panmyelóza s myelofibrózou |
| Myelosarkom |
Upraveno podle: Doubek M, Mayer J. Akutní myeloidní leukémie. In: Pospíšilová Š, Dvořáková D, Mayer J. et al. Molekulární hematologie. Praha, Galén, 2013; 209 – 224.
Prognostické faktory
Akutní myeloidní leukémie představuje značně heterogenní skupinu maligních onemocnění krvetvorby, s odlišnou prognózou a odpovědí na léčbu. Ta je ovlivněna nejen charakterem samotného onemocnění, ale také věkem pacienta a přidruženými chorobami. Zvyšující se věk je nepříznivým prognostickým faktorem, důležité je však také vyhodnocení komorbidit. Kalendářní věk není jediným kritériem rozhodujícím o léčebné strategii (starších) pacientů. Karyotyp leukemických buněk je nejsilnější prognostický faktor odpovědi na léčbu a přežití. Spolu s výsledkem molekulárně-genetického vyšetření umožňuje stratifikaci pacientů do 3 rizikových skupin – příznivá (např. AML s t(8;21) nebo inv(16)), intermediární (např. AML s t(9;11) nebo inv(16) s c-KIT mutací) a nepříznivá (např. AML s t(6;9) nebo inv(3)), které se vzájemně liší svou prognózou. Podrobnější informace o prognostické stratifikaci AML na základě cytogenetiky a molekulární genetiky přesahují rozsah tohoto článku, a zájemci je mohou najít v početných publikacích věnovaných této problematice.
Léčba
Při výběru vhodného léčebného režimu je potřebné zohlednit výsledky speciálních vyšetření kostní dřeně (cytogenetické a molekulárně-biologické), věk a celkový zdravotní stav pacienta. Základem terapie AML je chemoterapie. Jestliže je počet blastů v krvi při zahájení léčby vyšší než 100×109/l, začíná terapie tzv. předléčením. To začíná obvykle leukaferézami (separace blastů mechanicky speciálním zařízením) a následným podáváním hydroxyurey. Jinak se léčba zahajuje tzv. indukční terapií, při které se pacientovi podává kombinace 3 dávek cytostatika daunorubicin a 7 dávek cytostatika cytarabinu ve formě infuzí. Tato léčebná schéma se označuje jako ‘3+7’.Touto léčbou lze dosáhnout kompletní remise, tj. redukce blastů v kostní dřeni pod 5% a obnovení normální krvetvorby u 50-75% pacientů. Pokud indukční léčba nevedla k remisi, podává se další kombinace cytostatik, tzv. záchranná terapie. Avšak ani v případě úspěšného navození remise není možné léčbu definitivně ukončit pro přítomnost zbytkových leukemických buněk. Nastupuje etapa tzv. konsolidační léčby. Způsob této léčby závisí na prognostických faktorech (zejména genetické změny), zdravotním stavu pacienta, ale také na existenci vhodného dárce kostní dřeně v pacientově rodině, nebo v registru dobrovolných dárců. U nemocných starších 65-70 let nebo v případě závažných zdravotních komplikací znemožňujících podávaní kombinací cytostatik uvedených výše, volíme pouze symptomatickou léčbu, případně hydroxyureu a nízké dávky cytarabinu. Léčebná strategie se významně liší u pacientů s akutní promyelocytární leukemií (APL). Tento subtyp představuje asi 7% případů akutní myeloidní leukémie. Základem terapie APL je kombinace derivátu vitamínu A – all-transretinové kyseliny (ATRA) a antracyklinových cytostatik (idarubicin, resp. mitoxantron), bez nutnosti transplantace. APL je leukémie s velmi příznivou prognózou s možností vyléčení 75-85 % pacientů, je však důležité zvládnout v úvodu přítomné závažné krvácivé projevy, které mohou mít i fatální následky. Důležitou součástí komplexní terapie u pacienta s AML je také podávaní antiinfekčních přípravků jako prevence a léčba závažných infekcí, transfuzí červených krvinek a krevních destiček a také podpůrná psychologická terapie.
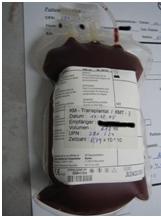
Obr. č. 5. (vlevo) Odběr kostní dřeně od dárce (autor: Andrew Ratto, www.wikipedia.org)
Obr. č. 6. (vpravo) Odebraná kostní dřeň připravená k podání pacientovi (autor: John Bergenholtz, www.wikipedia.org )
Prognóza
Neléčená AML končí vždy smrtí nemocného. Léčba přináší naději dočasného a u menší části pacientů trvalého vyléčení. U většiny pacientů, kteří dosáhli po chemoterapii remise, se leukémie vrátí do 3 let od diagnózy. Výsledek terapie závisí na genetickém podtypu leukémie, věku a použité léčbě. Neustále probíhající výzkum si klade za svůj cíl zlepšení prognózy a přežívaní pacientů s leukémií.
Praktické rady pro pacienty
AML je velice závažné onemocnění, které musí být vždy léčeno odbornými lékaři ve specializovaných centrech. Na možnou diagnózu leukémie je nutno při vyšetřování myslet a pacienta začít co nejdříve léčit. Jen tak lze zvýšit jeho šance na uzdravení. V případě jakýchkoliv pochybností by měl pacient vyhledat svého ošetřujícího lékaře, obzvláště při opakovaném výskytu infekcí špatně reagujících na antibiotika, či krvácení, které se u pacienta doposud neprojevovalo. Aktivní spoluúčast samotného pacienta při léčbě a víra v uzdravení jsou také nepostradatelnou součástí terapie akutní myeloidní leukémie.
Literatura
1.) Szotkowski T, Faber E. Akutní leukemie. In: Faber E. et al. Základy hematologické diagnostiky. 1. vyd. Olomouc, Univerzita Palackého v Olomouci, Lékařská fakulta, 2012; 153-159.
2.) Tošková M, Ráčil Z. Akútna myeloidná leukémia. Postgraduální medicína, 2011, 13, č.3
3.) Adam Z, Doubek M, Penka M. et al. In: Adam Z, Vorlíček J. et al. Hematologie II. Přehled maligních hematologických nemocí. 1. vydání. Praha, GradaPublishing, 2001; 37-49.
4.) Klener P. Akutní myeloidní leukémie. In: Klener P. et al. Vnitřní lékařství. 4. ,přepracované a doplněné vydání. Praha, Galén a Univerzita Karlova v Praze, 2011; 460-463.
5.) Bučková P, Buliková A, Cermanová M. Akutní myeloidní leukemie. Informace pro pacienty a jejich blízké. První vydání. Brno, Česká leukemická skupina – pro život (CELL), 2013
6.) Szotkowski T. Faktory prognózy akutní myeloidní leukemie. Olomouc, 2010. Doktorská dizertační práce. Lékařská fakulta Univerzity Palackého v Olomouci, Hemato-onkologická klinika.
7.) Schwarz J, Kačírková P, Markalová J. Urgentní stav v hematologii: akutní promyelocytární leukemie–principy diagnostiky. VnitřLék 2008; 54(7&8): 728–7448.) Žák P. Akutní promyelocytární leukémie. Postgraduální medicína, 3/2007
8.) Doubek M, Mayer J. Akutní myeloidní leukémie. In: Pospíšilová Š, Dvořáková D, Mayer J. et al. Molekulární hematologie. Praha, Galén, 2013; 209 – 224.
Zpracoval: Martin Čerňan, 1MUDr. Tomáš Szotkowski, Ph.D.
1Hemato-onkologická klinika LF UP a FN Olomouc