Charakteristika arteriálního krevního tlaku
Stálé nebo alespoň přibližně stálé hodnoty středního arteriálního tlaku jsou základním předpokladem účinné regulace průtoku krve periferií. Pouze za této podmínky se vytváří stálý tlakový spád a tlaková rezerva, které jsou nutné pro nezávislé rozdělování krve. Lokální změny průsvitu arteriol potom mohou mít předvídatelný účinek – zvýšit nebo snížit průtok krve tkáněmi. Regulace krevního tlaku proto je zaměřena především na udržení stálého středního systémového arteriálního tlaku.
Primární a sekundární hemodynamické veličiny
V úzkém hemodynamickém pojetí ustáleného oběhu jsou bezprostředními determinantami systémového arteriálního tlaku srdeční výdej J a celková periferní rezistence R. Střední arteriální tlak P může být popsán rovnicí P = J x R. Tato rovnice je nedocenitelným klasickým nástrojem popisu krátkodobých regulačních zásahů.
Přesto je při aplikaci rovnice nutno pamatovat na její omezení. Formální matematický způsob čtení rovnice navádí vidět P jako závisle proměnnou a J a R jako nezávisle proměnné. Fyziologická realita je jiná. Z fyziologického hlediska je tlak P v systémovém oběhu nezávislou, primární veličinou cirkulace, dlouhodobě determinovanou ledvinovým přepadem. Podobně i odpor R je primární, nezávislou hemodynamickou veličinou, dlouhodobě určovanou lokální autoregulací ve tkáních. Sekundární, závisle proměnnou hemodynamickou veličinou je srdeční výdej J. Fyziologický popis dlouhodobých oběhových stavů a chronických poruch oběhu proto musí upřednostňovat hemodynamickou rovnici ve tvaru J = P/R.
Měření krevního tlaku
- Neinvazivní měření arteriálního tlaku se rutinně provádí třemi metodami. Všechny využívají sfygmometrický princip (registraci tepu po uvolnění nafouknuté manžety:
- Sfygmomanometricky – nafouknutou mažetou se rtuťovým tonometrem s fonendoskopem, určují se Korotkovovy fenomény;
- Oscilometricky – oscilace po uvolnění nafouknuté manžety se detekují zařízením umístěným nad arterií;
- Dopplerovskou technikou – snímá se pohyb krve sondou umístěnou nad arterií.
- Invazivní měření
- Jsou nezastupitelné při těžké hypotenzi, významném poklesu srdečního výdeje anebo při špatné dosažitelnosti signálu arterií z povrchu (mimořádná obezita, rozsáhlé otoky).
Určení středního arteriálního tlaku
Střední arteriální tlak (MAP, mean artrerial pressure) není prostým průměrem systolického (sAP) a diastolického (dAP) tlaku, ale rutinně se počítá podle vzorce
- MAP = (sAP + 2 x dAP)/3.
Pokles MAP pod 70 mm Hg, nebo náhlý pokles MAP o ≥ 40 mm Hg jsou známkou cirkulačního selhání.
Perfúzní tlak
Arteriální tlak je determinantou krevního proudu procházejícího mikrocirkulací z artérií do venózního systému. Perfúzní tlak PP je roven rozdílu tlaků na začátku a na konci mikrocirkulace; v nejširším pojetí:
- PP = MAP – CVP (CVP, centrální venózní tlak).
Hodnoty PP < 65 mm Hg ukazují na cirkulační selhání.
Arteriální a pertúzní tlak orientačně informují o perfúzi orgánů. Nevypovídají však o její kvalitě. Při vazokonstrikci např. může být MAP normální a tkáně přesto mohou trpět hypoxií.
Regulace arteriálního krevního tlaku
Střední systémový plnicí tlak v krevním řečišti odráží poměr mezi kapacitou řečiště a náplní v něm, podobně jako je tomu v míči nebo v pneumatice. Tento poměr se může změnit dvěma způsoby:
- Snížením, nebo zvýšením kapacity cirkulace;
- Zmenšením, nebo zvětšením objemu krve.
Prostřednictvím změn kapacity cirkulace působí všechny rychlé, poplachové anebo nouzové regulace. Tak při ztrátě krve a poklesu tlaku nastává reflexní vazokonstrikce a redistribuce (centralizace) krevního oběhu. Naopak, při infúzi tekutiny provázené zvýšením intrtavaskulárního objemu a tlaku dochází k reflexní vazodilataci. Jinými slovy, pohotovostní, krátkodobé regulační mechanismy přizpůsobují kapacitu cirkulace její náplni. Tím zmírňují dopady kolísání objemu krve na krevní tlak.
Na druhé straně dlouhodobé regulace využívají alternativní způsob – mění objem krve v cirkulaci. Jsou relativně pomalé, ale dovedou to, co poplachové systémy neumí – úplně a beze zbytku přizpůsobí náplň cirkulace její kapacitě.
Střední systémový plnicí tlak určuje plnění srdce, a tím srdeční výdej, který je jednou z bezprostředních determinant systémového arteriálního tlaku (P = J x R). Systémová arteriální hypertenze neboli hypertenzní nemoc je podle definice dlouhodobým, chronickým onemocněním. Při této hypertenzi tudíž musí být v centru pozornosti právě dlouhodobé mechanismy regulace tlaku a jejich poruchy.
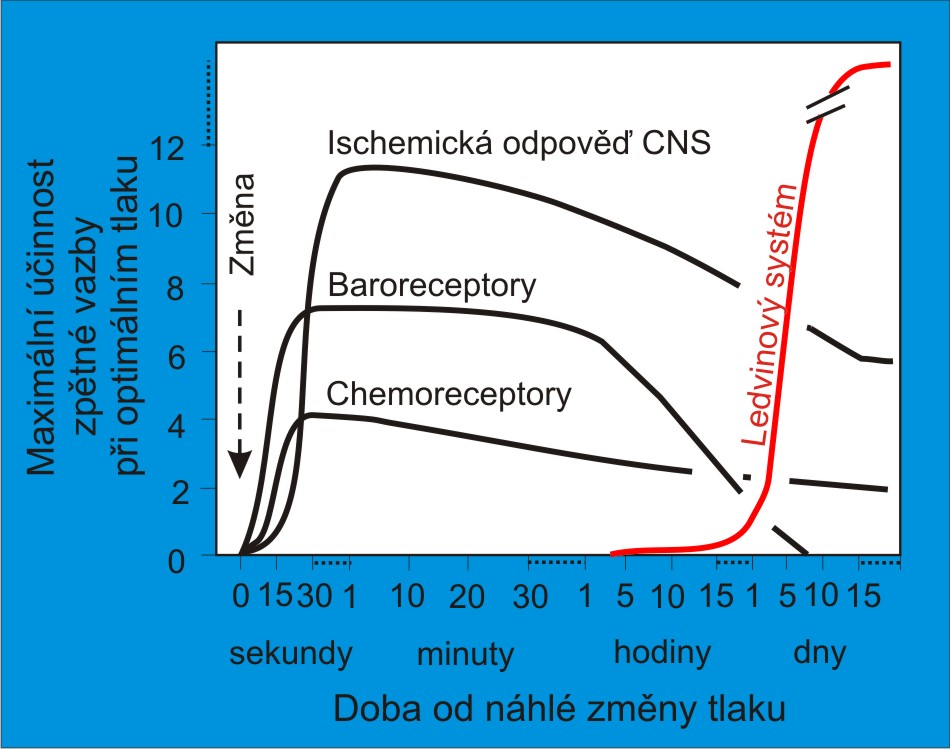
Mechanismy kontroly arteriálního tlaku se dělí do tří skupin podle rychlosti nástupu jejich účinků a doby jejich trvání (obr. 1):
- Krátkodobé mechanismy;
- Střednědobé mechanismy;
- Dlouhodobé mechanismy.
Obr. 1. Přehled mechanismů regulace krevního tlaku. Věnujte prosím pozornost adaptaci (vyhasínání) krátkodobých regulačních mechanismů. Nejsou znázorněny střednědobé mechanismy. Bližší údaje jsou uvedeny v textu. (Podle AC Guyton a JE Hall: Textbook of Medical Physiology, 11th Ed. Elsevier/Saunders, Philadeplhia. 2006.) Schéma je možno zhlédnout i v animované podobě.
Krátkodobé mechanismy
Krátkodobé mechanismy rozvíjejí svou účinnost do plné intenzity v průběhu sekund anebo minut. Jde v první řadě o nervové mechanismy kontroly tlaku – o baroreceptorový a chemoreceptorový reflex a o tzv. ischemickou odpověď centrálního nervového systému (obr. 1). Lze sem přiřadit i reflexní odpovědi, které vycházejí z receptorů napětí (receptorů nízkého tlaku v srdečních síních a v pulmonálních arteriích, včetně reflexů Bainbridgeova a Bezold-Jarischova).
Pohotovostní, krátkodobá kontrola tlaku má rychlý nástup, ale časově omezenou účinnost. Baroreceptory vystavené nové úrovni krevního tlaku se na ni adaptují v průběhu asi tří dnů (obr. 1). Poté se „pufrování“ tlaku děje v relaci k nové hodnotě, na kterou se receptory adaptovaly. Baroreceptory reagují spíše na rychlost změny tlaku než na déletrvající změnu jeho hladiny. Jejich odpověď navíc slábne s tím, jak se korigovaná veličina blíží zpátky k normě. Proto nemohou zprostředkovat úplnou nápravu změny, k níž došlo.
V krátkodobé regulaci se uplatňují i některé humorální mechanismy. Především jde o katecholaminy adrenalin a noradrenalin vyplavené po sympatické stimulaci z dřeně nadledvinek. Prodlužují a potencují účinek přímého nervového zásobení cév. Navíc působí i v místech, kde je nervové zásobení chabé, např. v oblasti metaarteriol a venul. Poločas katecholaminů v cirkulaci je asi 3 minuty.
Střednědobé mechanismy
Střednědobé působící mechanismy rozvíjejí své účinky do plné intenzity od desítek minut do několika hodin. Patří sem relaxace cévní stěny při změnách krevního tlaku a přesuny tekutin mezi intra- a extravazálním prostorem v kapilárním úseku cirkulace.
Z humorálních mechanismů se ke střednědobým mechanismům řadí především systémové vazokonstrikční působení dvou faktorů, a sice angiotenzinu II a antidiuretického hormonu neboli vazopresinu.
Dlouhodobé mechanismy
Pro funkce, které má cirkulace plnit, je rozhodující stálý arteriální krevní tlak. Je hybnou silou cirkulace a zajištění přísunu živin do tkání. V dlouhodobé perspektivě lze dosáhnout setrvalých hodnot tlaku pouze přizpůsobením objemu náplně cirkulace její kapacitě. Dlouhodobá regulace arteriálního tlaku proto na rozdíl krátkodobých a střednědobých mechanismů přímo souvisí s regulací objemu tělesných tekutin.
Pokud zůstává zachována normální koncentrace plazmatických proteinů a není porušena celistvost oběhu, objem krve věrně odráží objem extracelulární tekutiny. Pokud jde o intracelulární prostor, výměnu tekutin mezi cytoplazmou a extracelulárním prostředím si regulují buňky samy. Nejsou známy žádné receptory, které by bezprostředně monitorovaly hladinu zásob tekutin v těle. Nejsou známy ani žádné receptory, které by přímo informovaly o absolutní velikosti náplně cirkulace. Tělo poměřuje velikost náplně nepřímo – hladinou arteriálního tlaku. Pokud existuje dlouhodobý soulad mezi náplní a kapacitou krevního řečiště, je setrvalá i úroveň arteriálního tlaku.
Dlouhodobé mechanismy zabezpečují úroveň tlaku úpravami objemu cirkulující krve. Přizpůsobují objem tekutiny v cirkulaci kapacitě krevního řečiště. V tom spočívá jejich diametrální odlišnost od krátkodobých a střednědobých mechanismů, které operují se změnami kapacity řečiště. (Jedinou výjimkou jsou přesuny tekutiny mezi extra- a intravazálním prostorem, uvedené mezi střednědobými mechanismy, které však mají jasný limit.)
Výkonným orgánem dlouhodobě působících mechanismů jsou ledviny (obr. 1). Ledviny nesou veškerou tíhu starosti za vyrovnanou bilanci tekutin v těle. Objem tekutin v těle a náplň cirkulace během dne silně kolísají se změnami příjmu a výdeje tekutin. Aby ledviny mohly zajistit vyrovnanou bilanci, musí být perfundovány v dostatečné míře a pod určitým tlakem. Ledviny jsou jediným orgánem v těle, který si dostatečnou perfúzi dokáže vynutit. Jsou pro to vybaveny mimořádně výkonnými metabolickými nástroji. Tato schopnost determinuje ledviny jako tělní orgán, jenž dlouhodobě určuje tlak v cirkulaci. Mohou diktovat hladiny arteriálního tlaku, jimž se nakonec podřizuje celý oběh. Arteriální tlak zpětně ovlivňuje exkreci vody a sodných iontů ledvinami. Tím se vytváří přímé spojení mezi cirkulací a homeostázou tělních tekutin a sodných iontů. Obecně se hovoří o ledvinovém systému dlouhodobé regulace arteriálního tlaku a dlouhodobé bilance tělních tekutin. Má řadu intraparenchymálních ledvinových i mimoledvinových funkčních článků. Tím, že kontroluje intravaskulární volum a dokáže kompenzovat nesoulad mezi kapacitou řečiště a velikostí jeho náplně, má fundamentální postavení v udržování dlouhodobých hladin krevního tlaku.
Pokud není funkce ledvin porušena, je kompenzační schopnost dlouhodobých mechanismů – na rozdíl od mechanismů obou výše uvedených skupin – téměř neomezená. Zdravé ledviny se na změny arteriálního tlaku neadaptují a obnovují normální hladinu tlaku, dokud nedosáhnou její úplné úpravy. Zatímco krátkodobé a střednědobé mechanismy časem slábnou, kompenzační odpověď dlouhodobých ledvinových mechanismů s časem roste. I v tom tkví jedinečné postavení a patofyziologický význam ledvinového systému v regulaci tlaku.
Tlaková diuréza a ledvinová funkční křivka
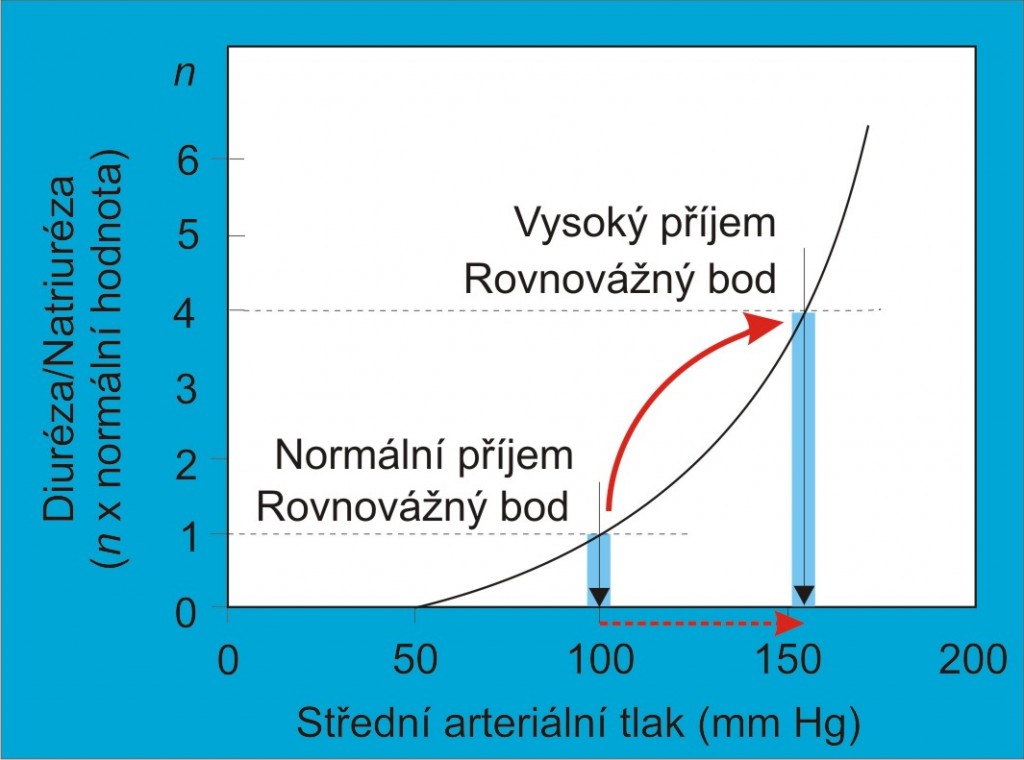
Mechanismem, jímž ledviny přizpůsobují objem krve kapacitě cirkulace, je tlaková diuréza. Spočívá v tom, že ledviny při zvýšení arteriálního tlaku zvýší výdej tekutin a soli a při poklesu arteriálního tlaku omezí výdej tekutin a soli. Grafickým vyjádřením je křivka tlakové diurézy neboli renální funkční křivka.
Obr. 2. Křivka tlakové diurézy/natriurézy neboli ledvinová funkční křivka. Čárkovaně je vyznačena křivka tlakové diurézy provázející zvýšenou resorpci (sníženou exkreci) sodných iontů a vody v tubulech např. při hypovolémii. (Podle AC Guyton a JE Hall: Textbook of Medical Physiology, 11th Ed. Elsevier/Saunders, Philadeplhia. 2006.) Schéma je možno zhlédnout i v animované podobě.
Ledviny za fyziologických okolností při vzestupu arteriálního tlaku prakticky okamžitě zvýší tvorbu moči – asi 30 – 60 s poté, co došlo ke změně tlaku. Při vzestupu středního arteriálního tlaku asi o 15 % (tj. o 10 – 20 mm Hg) se diuréza zdvojnásobí.
Teorie tlakové natriurézy, jejího výsadního postavení v dlouhodobé regulaci objemu tělesných tekutin a krevního tlaku, a spolu s tím i teorie určující úlohy poruch tlakové diurézy v hypertenzi, se opírá o množství experimentálních a klinických dat. Všechny experimetnálně vyvolané hypertenze vznikají po zásazích do struktury anebo funkce ledvin. U všech forem hypertenze – experimentálních i klinických, sekundárních i primárních, sůl-senzitivních i sůl-nesenzitivních –, které zatím byly zkoumány, byla prokázána přítomnost abnormální renální funkční křivky. Není známa žádná hypertenze, u níž by základní funkční vztah mezi arteriálním (perfuzním) tlakem a natriurézou zůstal neporušen.
Původ chronických odchylek středního systémového arteriálního tlaku od normy
Trvalé odchylky středního systémového arteriálního krevního tlaku od normálních hodnot se objevují pouze tehdy, když dochází k dlouhodobému nepoměru mezi náplní krevního řečiště a jeho kapacitou. V klinice se setkáváme s chronickou systémovou arteriální hypertenzí (hypertenzní nemocí) a – mnohem méně často – s chronickou systémovou arteriální hypotenzí. Obecné příčiny chronického zvýšení tlaku mohou být dvojí (pomíjí se pružníková, tedy izolovaná systolická hypertenze):
- Dlouhodobý nárůst objemu intravazální tekutiny bez náležité změny kapacity cirkulace.
- Dlouhodobé zmenšení kapacity cirkulace bez náležitého zmenšení objemu krve.
V obou případech jde o poruchu přizpůsobení náplně cirkulace její kapacitě, za které jsou odpovědné ledviny.
Dlouhodobé poruchy tlakové diurézy
Každé porušení křehké rovnováhy faktorů určujících exkreční funkce, kterými ledviny zabezpečují vyrovnanou bilanci iontů a tekutin, způsobí poruchu přizpůsobení náplně cirkulace její kapacitě. Porucha se v grafickém znázornění projeví posunem anebo změnou sklonu renální funkční křivky. Pokud se při stálém příjmu iontů sodíku a vody křivka posune nebo skloní doprava, k vyšším hodnotám krevního tlaku, vyvine se exkreční deficit. Stávající tlak nebude schopen zajistit dostatečnou tlakovou diurézu a z těla se nebude moci vyloučit dostatečné množství přijatých iontů a tekutin. Dojde k jejich akumulaci, k expanzi extracelulárního prostoru, a zvýší se střední systémový plnicí tlak (obr. 3).
Obr. 3. Posun hladiny středního systémového arteriálního krevního tlaku při skloněné funkční křivce ledvin, kdy diuréza (natriuréza) není schopna zajistit vyrovnanou bilanci objemu tekutin. (Podle AC Guyton a JE Hall: Textbook of Medical Physiology, 11th Ed. Elsevier/Saunders, Philadeplhia. 2006.)
Pokud za takových okolností organismus nemá zaniknout, musí dohnat exkreční deficit a obnovit vyrovnanou bilanci iontů sodíku a vody. Vzhledem k existenci mimořádně těsného spřažení diurézy s krevním tlakem se stav může napravit pouze za cenu zvýšení arteriálního tlaku. Jestliže jsou změny v ledvinách dlouhodobé, nebo dokonce nevratné, krevní tlak se musí trvale obětovat uvedenému cíli. Ledviny, jejichž funkce se řídí přísnými zákonitostmi vyrovnané bilance tekutin, vnutí cirkulaci hypertenzi. Ustálí nový systémový arteriální tlak, a to přesně na té úrovni, při které budou schopny udržet vyrovnanou bilanci. Ilustrativním učebnicovým příkladem neomezené kapacity ledvin, pokud jde o to, podřídit jejich potřebám hemodynamické poměry, je vysvětlení fenoménu úniku.
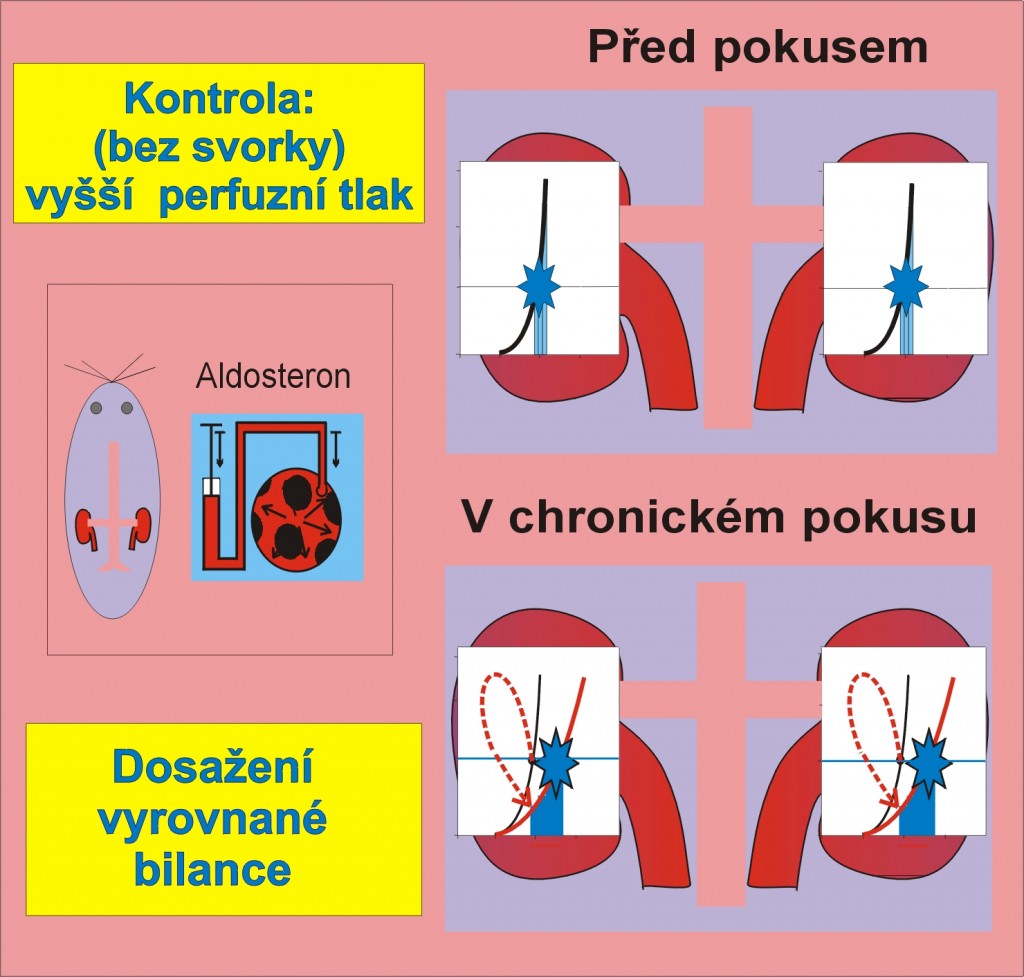
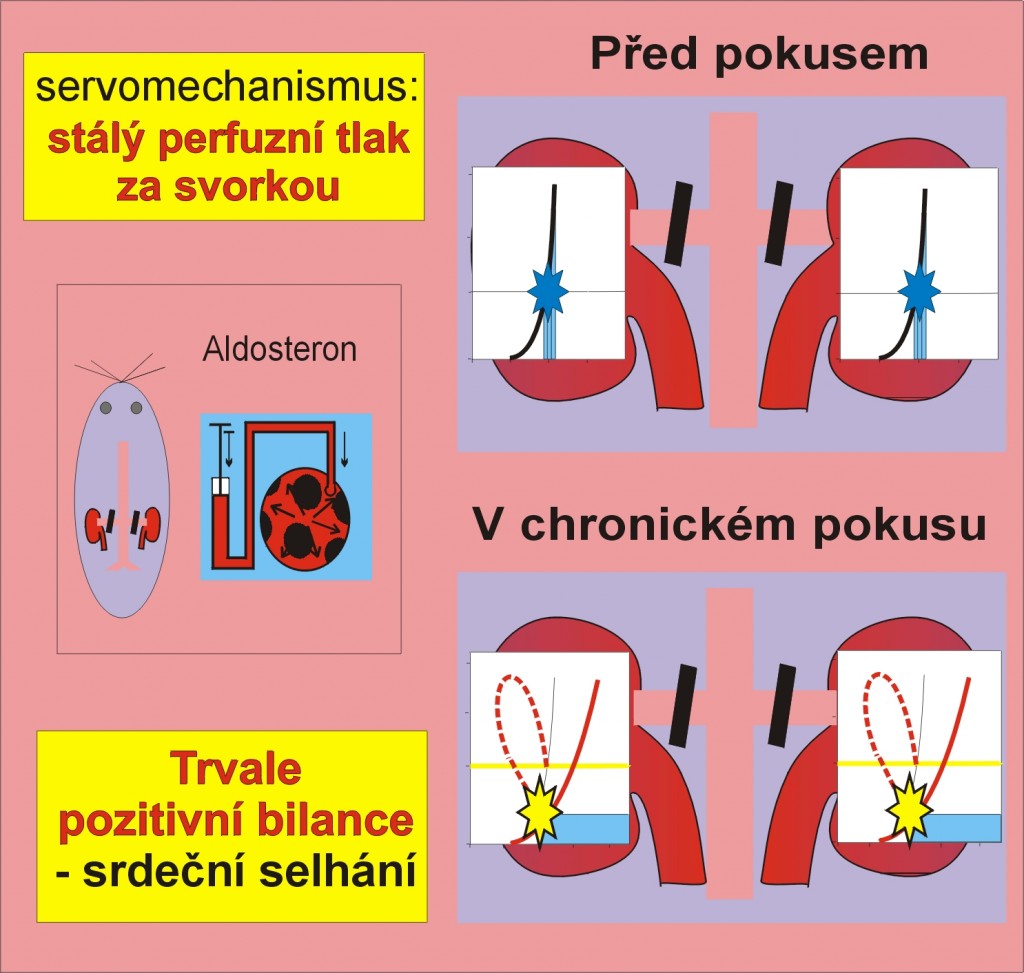
Experimentální objasnění úlohy ledvinového perfúzního tlaku ve fenoménu úniku. Pro vyjasnění úlohy, kterou mají ve fenoménu úniku ledviny, bylo experimentálním zvířatům instalováno na renální arterie zařízení, které dovolovalo kontrolovat renální perfúzní tlak. Tímto zařízením byl perfúzní tlak udržován na výchozích (normálních, nezvýšených) hodnotách. Za pozornost stojí dvě situace:
- U kontrolních jedinců, u nichž zařízení nebylo instalováno a kterým byl aldosteron dodáván v infúzi po 7 dní, měl experiment obvyklý průběh. V prvních 3 – 4 dnech se akumulovaly ionty Na+, mírně se zvýšil střední arteriální a renální perfúzní tlak. Potom se akumulace iontů a vzestup tlaku zastavily, a i když zůstaly zvýšené, obnovila se vyrovnaná iontová a vodní bilance (obr. 4).
Obr. 4. Experiment ilustrující únikový fenomén. Kontrolní pokus s chronickou infúzí aldosteronu bez naloženého servomechanismu. Dosažení vyrovnané bilance.
- V protikladu k tomu u zvířat, u nichž renální zařízení v průběhu infúze udržovalo perfúzní tlak na stálé výchozí (nezvýšené) hodnotě, se vyvinula těžká retence sodných iontů. Byla provázena výraznou hypertenzí. Někdy se objevily masivní otoky a další známky městnavého selhání (obr. 5). Tato situace napodobuje klinický průběh srdečního selhání, kdy srdce není schopno zvýšit arteriální tlak – a tedy perfúzní tlak v ledvinách – na potřebnou výši tak, aby se deaktivoval renin-angiotenzin-aldosteronový systém. (Pokud to dokáže, přeruší se další akumulace iontů sodíku, obnoví se vodní a solná rovnováha a růst otoků se zastaví – jako v kontrolním experimentu.)
Obr. 5. Experiment ilustrující únikový fenomén. Pokus se zařízením instalovaným na renální artérii, které v průběhu infúze aldosteronu nedovolilo zvýšit perfúzní tlak v ledvinách. Vyrovnaná bilance nebyla dosažena, vyvinulo se objemové srdeční selhání.
- Když se ovšem v kritické městnavé fázi experimentu zmíněné zařízení z renálních arterií odstranilo a tlak v ledvinách se srovnal se zvýšeným tlakem v ostatním systémovém oběhu (tj. perfúzní tlak v ledvinách vzrostl), promptně se dostavila diuréza a příznaky městnání rychle ustoupily. Arteriální tlak i kumulace sodných iontů se pak ustálily na mnohem nižších hodnotách, jež odpovídaly hladinám aldosteronu v cirkulaci. Zcela shodné poznatky přinesly i experimenty s infúzemi angiotenzinu II, antidiuretického hormonu anebo katecholaminů.
Lze shrnout, že objasnění fenoménu úniku spočívá v účinnosti tlakové diurézy. Rozhodujícím faktorem pro únik diurézy zpod kontroly natrium- a vodu šetřících hormonů je zvýšení renálního perfuzního tlaku. Tlak roste jen tak dlouho, dokud tlaková natriuréza nevyrovná retenční účinky hormonů.
Závěry
Z rozborů průběhu funkční křivky ledvin a jejích změn vyplývá, že trvalé zvýšení systémového arteriálního krevního tlaku mohou způsobit pouze dva druhy procesů:
- Dlouhodobá pozitivní bilance iontů sodíku a tekutin z jejich nedostatečného vylučování při dlouhodobých poruchách funkce ledvin. Takové poruchy se budou manifestovat patologicky změněnou renální funkční křivkou. Křivka bude trvale posunuta anebo skloněna doprava směrem k vyšším hodnotám arteriálního tlaku.
- Dlouhodobá pozitivní bilance iontů sodíku a tekutin z jejich trvalého nadměrného přívodu, kdy rychlost přírůstku objemu solí a tekutin bude přesahovat rychlost jejich výdeje.
Oba mechanismy se mohou kombinovat.
Analogické změny v opačných směrech směru mohou vést k chronické systémové arteriální hypotenzi.
Žádná jiná změna než chronická změna tlakové diurézy nemůže navodit trvalou alteraci hodnot středního systémového arteriálního tlaku.
Poruchy exkrece iontů sodíku anebo tekutin v ledvinovém systému mohou být vyvolány nejrůznějšími patologické zásahy. Podle původu je lze dělit na poruchy:
- Intraparenchymální (např. poruchy cévního zásobení, glomerulů, tubulů).
- Extraparenchymální (např. hypersekrece natrium- aněbo vodu-šetřících hormonů, zvýšená aktivita sympatického autonomního systému atd.).
Poruchy ledvinové funkční křivky jsou podrobně popsány v kapitole Hypertenzní nemoc – Systémová arteriální hypertenze.
Zpracoval: Jaroslav Veselý, Ústav patologické fyziologie LF UP v Olomouci
Při tvorbě této stránky byl se svolením autora a vydavatele částečně využit text monografie „Tlaková diuréza a arteriální hypertenze“ (Autor: J. Veselý. Vydavatelství EPAVA, Olomouc. 2002). V případě zájmu o původní širší text prosím kontaktujte vydatelství EPAVA, Olomouc (E-mail: ec@epava.cz).