Charakteristika
Zjištění viability myokardu má klinický význam u pacientů s dysfunkcí levé komory a nízkou EF levé komory (EF pod 40 %). Signifikantně horší prognózu mají nemocní s dysfunkčním viabilním myokardem, nejsou-li revaskularizováni, než ti, kteří se podrobili revaskularizaci anebo než nemocní s dysfunkčním neviabilním myokardem.
Tabulka 1. Indikace SPECT (jednofotonové emisní počítačové tomografie) zobrazování myokardu
| Detekce, lokalizace, rozsah a závažnost myokardiální ischémie |
| Stratifikace rizika, posouzení závažnosti stenózy zjištěné při koronarografii |
| Vyšetření po koronární revaskularizaci (angioplastika nebo bypass) |
| Zjištění viability myokardu u pacientů s dysfunkcí levé komory při plánování revaskularizace |
| Kvantifikace funkce levé komory (alternativa k echokardiografii nebo ventrikulografii) |
Klinické hodnocení
Intervenční kardiology zpravidla zajímá nejen viabilita, ale také rozsah a závažnost ischémie v jednotlivých koronárních povodích. Proto se nejcennějším testem jeví zátěžové SPECT vyšetření, které poskytne odpověď na obě otázky. Pokud je klinický dotaz pouze na viabilitu, nebo pacient není schopen zátěže, lze provést jen klidové SPECT vyšetření. Dysfunkční segmenty s fixním defektem vychytávajícím méně než 50 % maximální aktivity perfúzního radiofarmaka odpovídají jizvě po infarktu myokardu (obrázky 1 a 2A-C). Pokud v dysfunkčním segmentu zobrazíme zhoršenou perfúzi, ale vychytávání radiofarmaka je ještě nad hranicí 50 % maxima, hovoříme o hibernujícím myokardu (obrázek 3). Nález normální perfúze v dysfunkčním segmentu svědčí pro omráčený myokard.
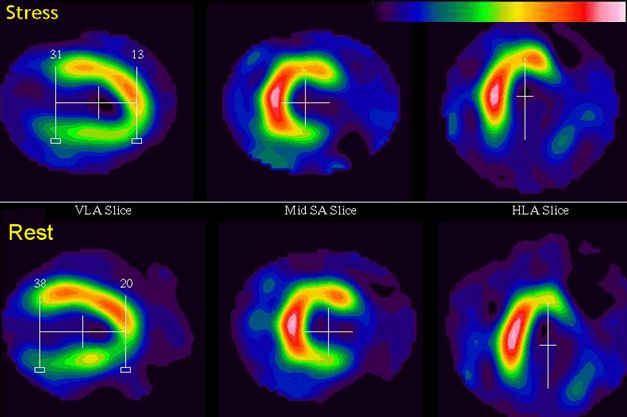
Obr. 1 Fixní defekt perfúze s nízkou akumulací radiofarmak u 54letého pacienta svědčí pro jizvu po infarktu myokardu v oblasti bočné stěny.
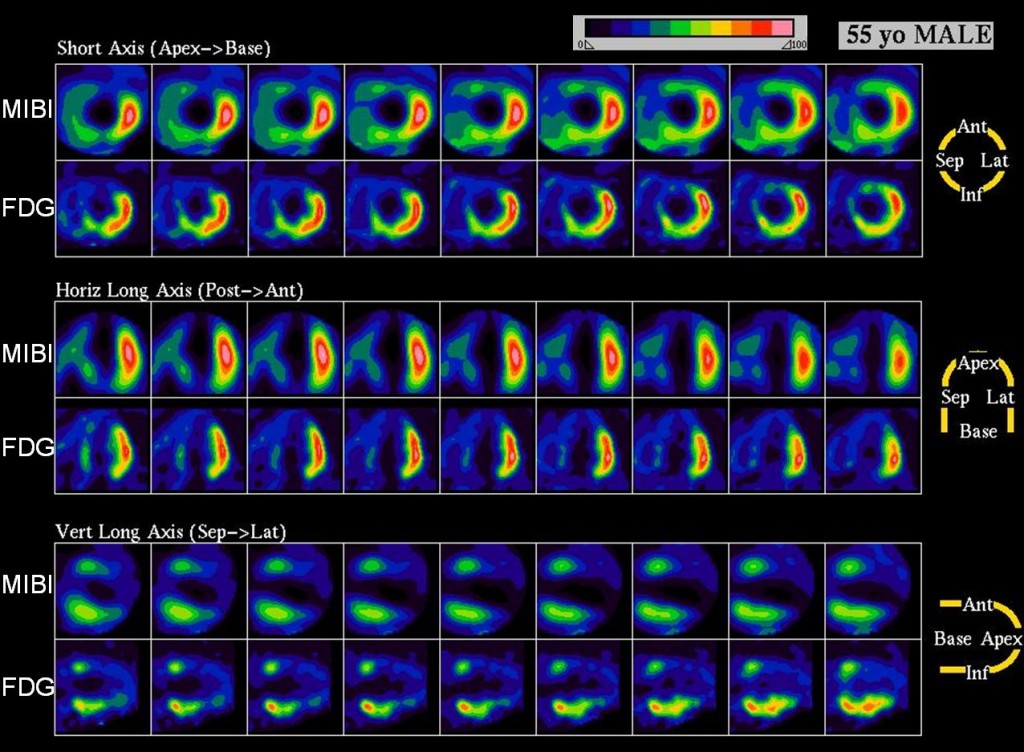
Obr. 2A 55letý muž s akutním anteroextenzivním infarktem myokardu léčeném direktivní perkutánní koronární intervencí (PCI) na ramus interventricularis anterior. Na tomografických řezech levé komory po aplikaci Tc-99-MIBI SPECT a F-18-FDG je v horizontální dlouhé ose zobrazen „perfúzně metabolický match“ svědčící pro jizvu anteriorně, anteroseptálně a apikálně.
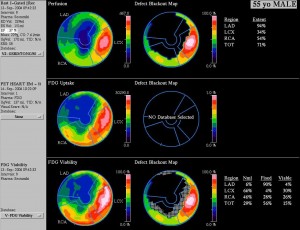
Obr. 2B Kvantifikace na polárních mapách u téhož pacienta svědčí pro rozsáhlý neviabilní myokard postihující 56 % levé komory a 90 % povodí ramus interventricularis anterior (LAD).
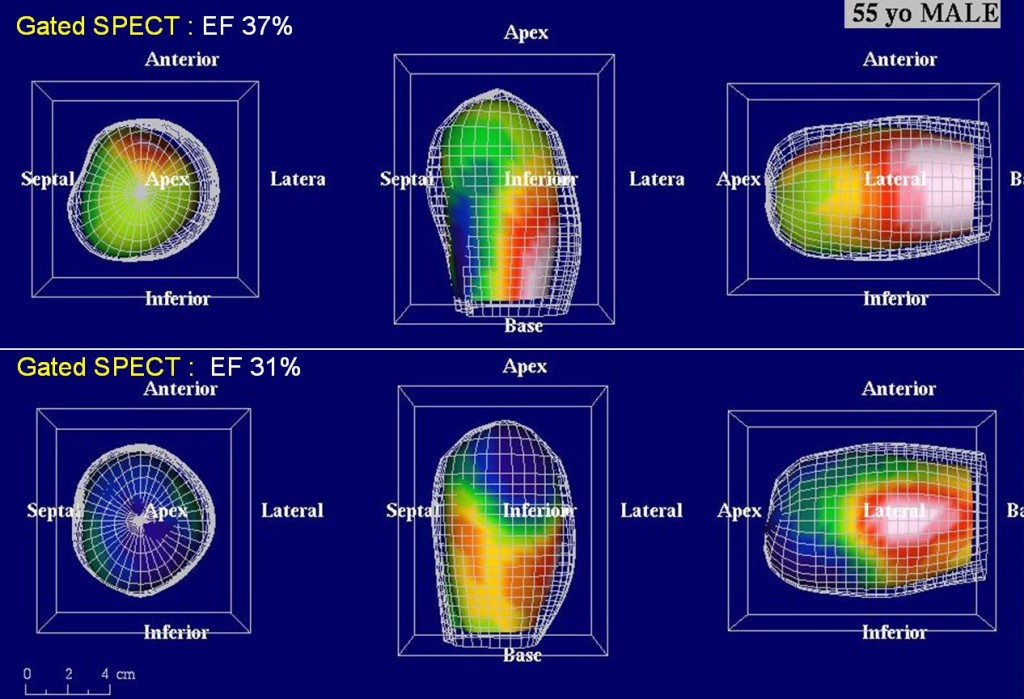
Obr. 2C Na gated SPECT bezprostředně po infarktu (horní řádek) je patrná hypokinéza přední stěny, septa a hrotu. Objemy levé komory byly výrazně zvýšené (EDV 239 ml, ESV 151 ml) a EF snížena na 37 %. Při kontrole za 3 měsíce po PCI (dolní řádek) je patrné, že regionální kinetika se nezlepšuje, naopak dochází k poinfarktové remodelaci s nárůstem objemů (EDV 299 ml, ESV 205 ml) a dalšímu snížení EF na EF 31 %.
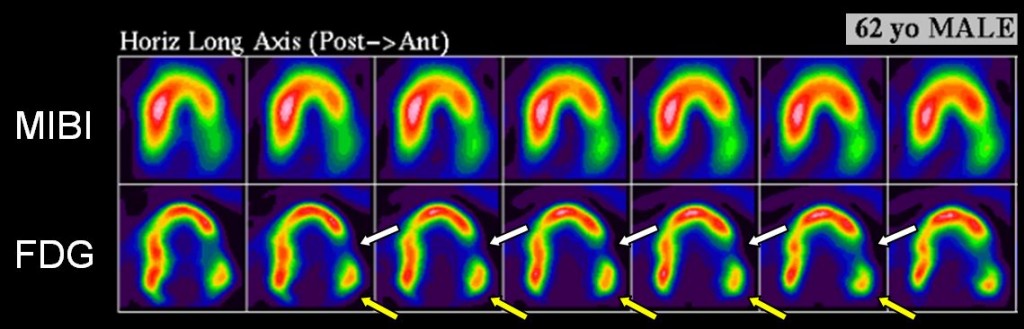
Obr. 3 62letý muž s průkazem hibernujícího myokardu v bazální partii bočné stěny (perfúzně-metabolický „mismatch“ – žluté šipky) a jen nevelkou oblastí neviabilního myokardu ve střední třetině bočné stěny (perfúzně-metabolický „match“ – bílé šipky).
Zpracoval: Milan Kamínek, Klinika nukleární medicíny LF UP a FN v Olomouci. Formálně upravil: Jaroslav Veselý, Ústav patologické fyziologie LF UP.
Literatura k dalšímu studiu:
- Hesse B, Tägil K, Cuocolo A, et al. EANM/ESC procedural guidelines for myocardial perfusion imaging in nuclear cardiology. Eur J Nucl Med Mol Imaging 2005;32:855-97.
- Germano G, Berman DS. Regional and Global Ventricular Function and Volumes from Single-Photon Emission Computed Tomography Perfusion Imaging. In: Zaret BL, Beller GA. Clinical Nuclear Cardiology. Third Edition. Philadelphia, Elsevier Mosby, 2005, 189-212.
- Kamínek M, Lang O, Henzlova M. Activity of nuclear cardiology in the Czech Republic in 2000 – 2005. Eur J Nucl Med Mol Imaging 2007;34:959-960.
- Underwood SR, Wiener S. Myocardial perfusion scintigraphy in Europe 2005: A survey of the European Council on Nuclear Cardiology. Eur J Nucl Med Mol Imaging 2009;36(2):260-268.
- Mysliveček M, Kamínek M. Doporučení k provádění zátěžových testů v nukleární kardiologii. Cor Vasa 2000;42(3): K54-56.
- Lang O, Kamínek M, Trojanová H. Nukleární kardiologie. Galén, Praha, 2008.
- Flotats A, Knuuti J, Gutberlet M, et al. Hybrid cardiac imaging: SPECT/CT and PET/CT. A point position statement by the European Association of Nuclear Medicine (EANM), the European Society of Cardiac Radiology (ESCR) and the European Council of Nuclear Cardiology (ECNC). Eur J Nucl Med Mol Imaging 2011;38:201–212.
- Klocke FJ, Baird MG, Lorell BH, , et al. ACC/AHA/ASNC guidelines for the clinical use of cardiac radionuclide imaging—executive summary: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (ACC/AHA/ASNC Committee to Revise the 1995 Guidelines for the Clinical Use of Cardiac Radionuclide Imaging). J Am Coll Cardiol 2003;42:1318–33.
- Hachamovitch R, Rozanski A, Shaw LJ, et al. Impact of ischaemia and scar on the therapeutic benefit derived from myocardial revascularization vs. medical therapy among patients undergoing stress-rest myocardial perfusion scintigraphy. Eur Heart J 2011;32:1012–1024.
- Metelková I, Kamínek M, Sovová E, et al. Stratifikace rizika pomocí zátěžového SPECT zobrazení myokardu v kombinaci se stanovením koronárního kalciového skóre u rizikových pacientů s diabetem a/nebo ledvinným selháním. Vnitř Lék 2010;56(11):1122-29.
- Budíková M, Kamínek M, Sovová E, Kaletová M, Metelková I, Henzlová L, Buriánková E, Formánek R. Prognostický význam koronárního kalciového skóre a zátěžového zobrazení myokardu pomocí jednofotonové emisní tomografie u asymptomatických rizikových pacientů. Cor Vasa (v tisku).
- Hendel RC, Abbott BG, Bateman TM, et al. The role of radionuclide myocardial perfusion imaging for asymptomatic individuals. J Nucl Cardiol 2011;18(1):3-15.
- Wijns W, Kolh P, Danchin N, et al. Guidelines on myocardial revascularization. Eur Heart J 2010;31(20):2501-55.